Profiling of Glycans by Capillary Electrophoresis

近畿大学 薬学部
薬品分析学研究室
教授
鈴木 茂生 博士(薬学)
糖鎖はタンパク質や脂質などと結合し、組織や細胞表面に分布して、様々な生理機能を担っている。近年、オミックス情報が医療や創薬に活用されているが、その全てに糖鎖が関わっている。
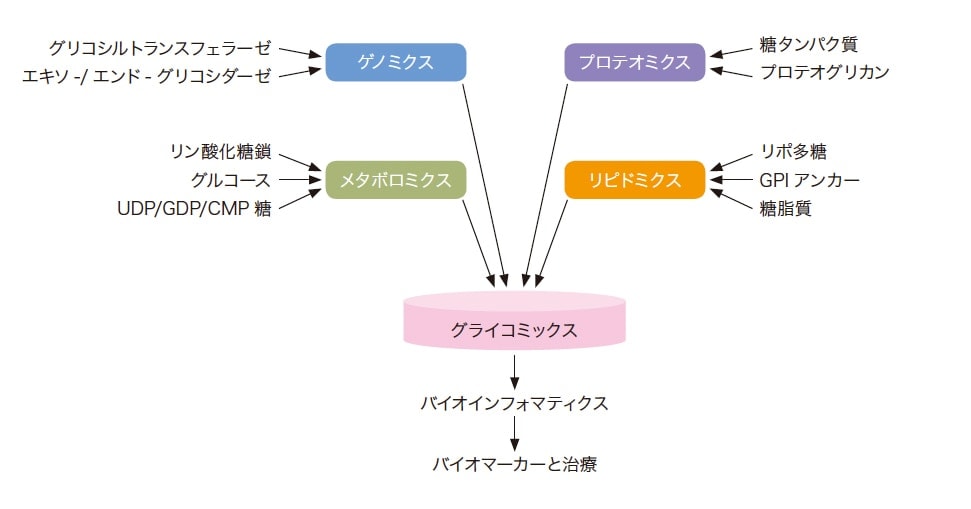
図1 オミックスと糖鎖情報(Hart, G. W.; Copeland, R. J. Cell 2010, 143, 672−676.より)
生体内で糖鎖や多糖複合体がどのような形で存在しているかを図2に示す。二糖単位の繰り返し構造をもつグリコサミノグリカンの多くはコアタンパク質と結合し、関節や皮膚の細胞外マトリックスとして身体の柔軟性を維持している。糖脂質は細胞膜の重要な構成要素である。さらにGPIアンカーは酵素などを細胞につなぎ止める役割をもつ。
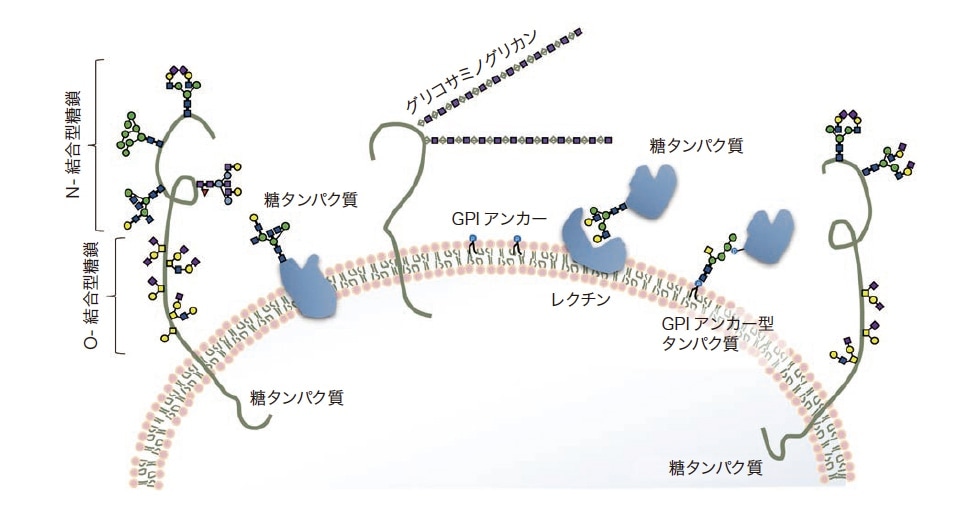
図2 細胞に存在する糖鎖の存在状態
ここでお話しする糖タンパク質の糖鎖はタンパク質のアスパラギン、またはセリンやトレオニンに結合し、それぞれ多様な構造を有する。糖タンパク質糖鎖の種類は数百種類と言われ、糖鎖と生理機能との関連は興味深い。
癌、アルツハイマー型認知症やハンチントン病など、重篤な疾患では病態の進行に伴って糖タンパク質の糖鎖構造が変化する。特定の糖鎖の出現や量的な変動はバイオマーカーとして診断の指標となる。近年ではバイオ医薬品が開発され、癌やリウマチ、C 型肝炎、糖尿病など、様々な難治性疾患の治療薬として、その市場規模は拡大しつつある。これら糖タンパク質製剤に付加する糖鎖の構造を制御することは難しく、細胞の選択や培養条件を糖鎖からも注意深く選抜する必要がある。特に非ヒト型糖鎖に含まれるN-グリコリルノイラミン酸やα - 結合ガラクトースはヒトでは遺伝的に欠損している。これら人体にとって免疫原性となる糖鎖の付加は生物製剤の価値を損なう危険性がある。
抗体医薬品が薬理効果を発揮するためには、本来の結合親和特異性に加えて、作用発現に重要なエフェクター機能として抗体依存性細胞障害活性(ADCC 活性)や補体依存性細胞障害活性(CDC 活性)が必要である。これらエフェクター活性と糖鎖の構造が関連している。したがって、抗体医薬品開発では、糖鎖構造の制御が重要な要素である。
糖タンパク質医薬品の有効性及び安全性を確保するためには、糖鎖の恒常性を確保することが重要である。しかし、糖鎖は小胞体からゴルジ体に分布する一連の糖関連酵素が協奏的に作用して合成されるので、糖鎖の生合成を制御することは極めて困難である。
糖タンパク質に結合している糖鎖の構造は多様で、結合部位によって糖鎖が異なることがある。さらに糖鎖構造は類似しているものが数多く存在し、その糖鎖の含量は4桁の幅があるといわれる。したがって、糖鎖解析を行う場合に、含量の下限をどこに設定するかで、データの質や作業効率は大きく異なる。
二次元ポリアクリルアミドゲル電気泳動などを用いて試料中のタンパク質を分子サイズや等電点に従って分離する。糖タンパク質のバンドを適切なプロテアーゼで消化し、得られた糖ペプチド混合物を液体クロマトグラフィー質量分析法(LC-MS)等により糖鎖結合部位ごとの糖鎖プロファイルを解析する。質量分析における糖ペプチドの感度は低く、イオン化条件にも依存する。そこで、通常は糖ペプチドから酵素(*1)や化学的手法(*2)によって糖鎖を遊離させる。また、糖含量が低い場合は、糖鎖を特異的に抽出(*3)する操作を加えることが多い。得られた糖鎖混合物は質量分析で解析することもあるが、糖鎖によって感度が異なる。そこで蛍光標識化を行って蛍光性の糖鎖誘導体に導き、HILICモードのHPLCなどで分析する(図4)。分離した糖鎖はピーク毎に回収され、エキソグリコシダーゼとMSn 解析やレクチンアフィニティー分析を組み合わせた構造推定ならびに1H-NMR や完全メチル化分析などを用いて、糖鎖構造を決定する。質量分析や蛍光検出の感度は高く、ピコ(10-12)モルオーダーの解析が可能である。一方、NMR は信頼性の高いデータを与える反面、マイクロ(10-6)モル量の精製した糖鎖を必要とする。
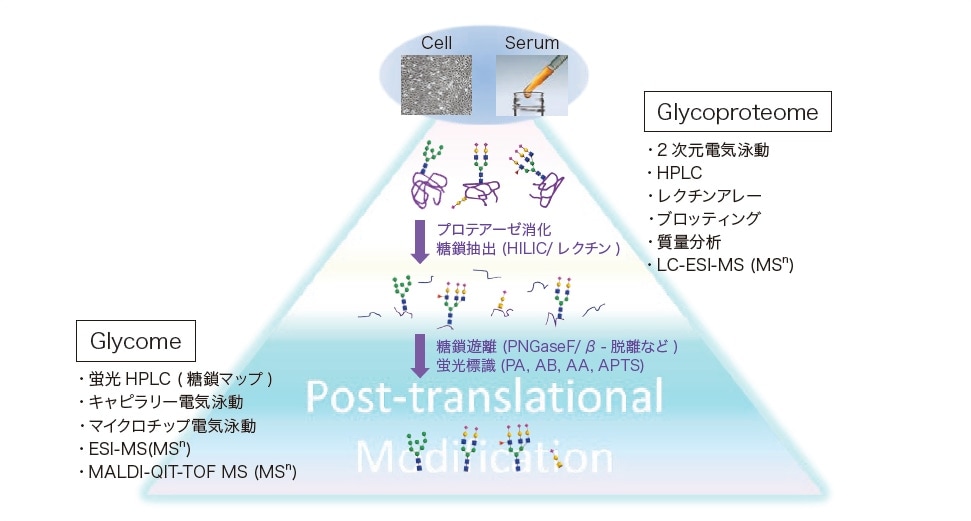
図3 グライコプロテオミクスの解析の流れと使用される分析技術
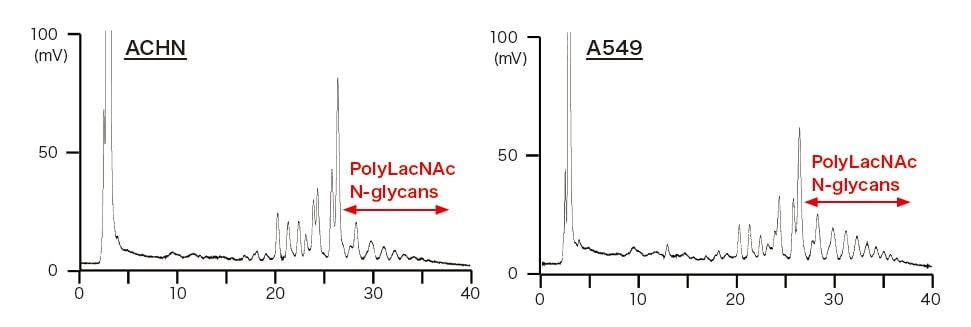
図4 2種類のがん細胞より調製したオリゴ糖の違い。糖鎖パターンは類似しているが糖鎖含量は異なる。
LC-MS をベースとする糖鎖プロファイル解析では個々の糖鎖構造を明らかにするために、糖鎖の特異的な濃縮、レクチン結合解析、エキソグリコシダーゼ消化などを組み合わせる必要がある。通常、存在量の大きな糖鎖だけを選んだとしても、数十種類の糖鎖をそれぞれ分画し、酵素反応をかけては分離という操作を繰り返さなければならない。また、質量分析における糖鎖の検出感度は低く、酸性糖鎖と中性糖鎖では測定モードを変える必要がある。
一方、糖鎖の還元的アミノ化による蛍光標識反応では糖鎖に1か所しか存在しない還元末端を蛍光剤で標識する。糖鎖の還元末端の構造は共通しているので、分離分析におけるピーク強度は糖鎖のモル分布を反映しており、定量的である。このことは、糖鎖の量やその増減を評価する上で極めて重要な特徴である。
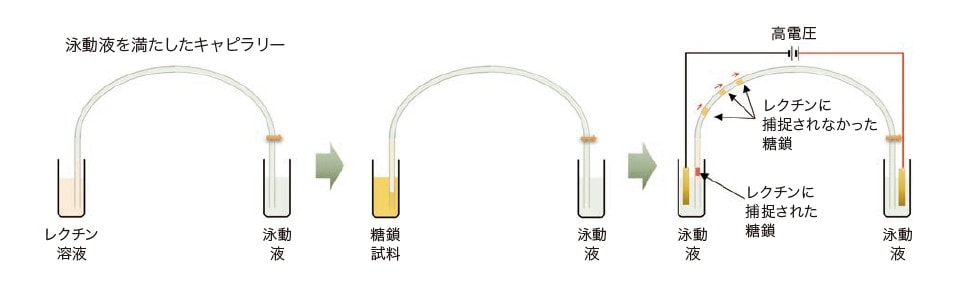
図5 レクチン部分導入キャピラリー電気泳動法の原理。レクチン溶液に続いて糖鎖試料を導入し、電圧を印加すると、マイナスの電荷をもつ糖鎖はレクチン層を通過し、一部の糖鎖が特異的にレクチンに捕捉される。
レーザー励起蛍光検出-キャピラリー電気泳動(LIF-CE)は高感度でハイスループットな糖鎖の定量的プロファイリングを可能にする。キャピラリー電気泳動の特性として高分離能を上げることが多いが、むしろ、その長所は中性の緩衝液でも良好な分離が得られるのでオンラインの酵素反応を併用できることに加え、試料が電荷当たりの分子サイズに応じて分離されるので、結果の解釈が容易な点にあると考えられる。例えば部分導入法(図5)では、キャピラリーの入口側(全長の1/10程度)に酵素や試薬の溶液を注入し、その後で試料を導入して、試料成分が酵素や試薬層を通過するように泳動させることで、反応生成物の分離パターンが得られる。我々は今までにレクチン(*3)やエキソグリコシダーゼ(*4)を本研究に用いたところ、レクチンごとの分離パターンから糖鎖構造の確認が可能であった。また、エキソグリコシダーゼを用いると、糖鎖は非還元末端側から消化されるので、反応後のオリゴ生成物を分離・検出できる。得られた分離パターンを標準糖鎖の分離データと比較すれば、かなり正確に存在する糖鎖を言い当てることができる。糖鎖分析では、糖鎖の含量分布が問題であるが、これに対して大規模濃縮法を応用することができる。すなわち、注入プログラムを変更するだけで、同じ試料を1,000倍近い感度で分析することができた。この方法を用いることで、キャピラリー電気泳動では0.1% 未満の微量の糖鎖でも特異的に観察することができる。
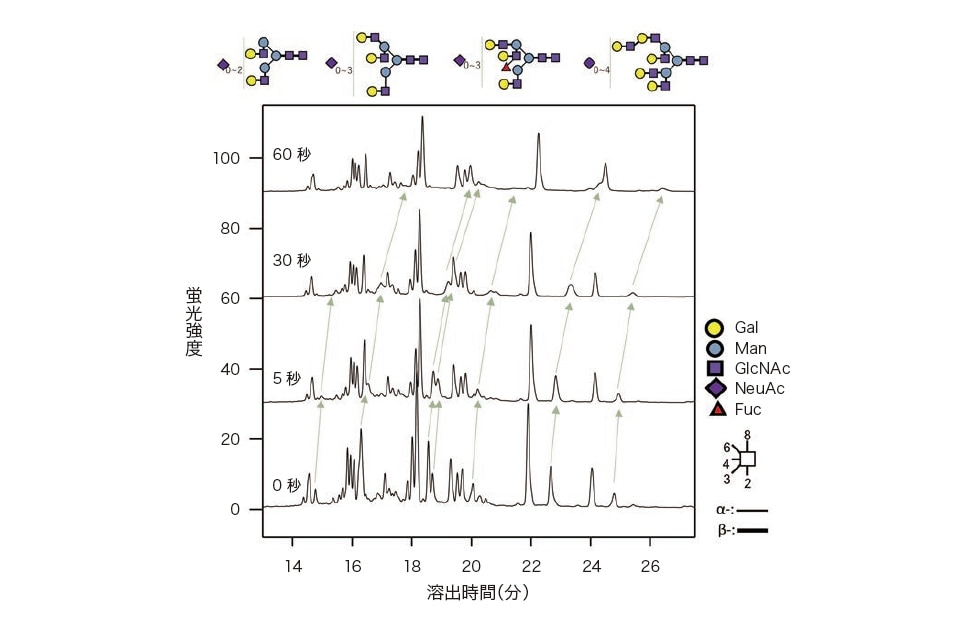
図6 部分導入キャピラリー電気泳動法でフコース認識レクチンの濃度を変えながら分析した例、レクチンの注入時間の増加とともにフコースが結合した糖鎖の保持時間が遅延している。
キャピラリー電気泳動は優れた糖鎖プロファイリング技術であることを述べた。ところが市販の装置はどれもキャピラリーの入口部分の温度制御ができない。そのため、予想されるよりも多量の酵素が必要であり、さらに糖鎖が酵素層を通過する間、電圧を下げて接触時間を増やすなど工夫が必要であった。部分導入法に適した装置が開発されれば、キャピラリー電気泳動の応用範囲が拡大し、糖鎖分析に限らず、様々な用途への適用が可能となる。是非、機器メーカーとして、本分野への参画を願っている。
脚注
さらに表示