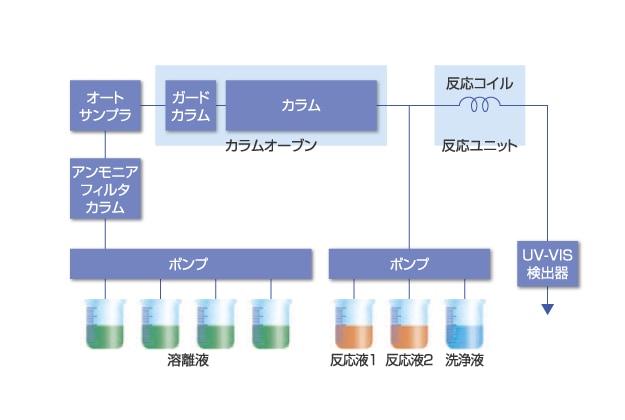
アミノ酸分析の原理と基礎
1. アミノ酸とは
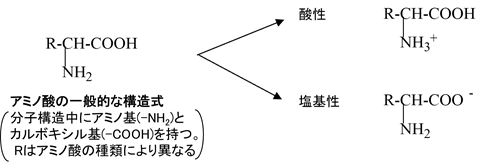
分子構造の中に-COOH(カルボキシル基)、-NH2(アミノ基)を有する有機化合物を総称してアミノ酸と呼びます。たん白質構成アミノ酸(約20種類)を含め、天然に存在するアミノ酸は約500種類ほどと言われています。
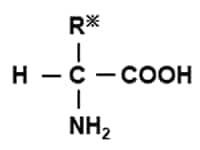
Rには独特な形をした基が結合します。
Rの性質により各アミノ酸の特性が異なります。
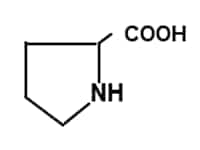
プロリンはアミノ基がイミノ基になっています。
環構造を持つため、他のアミノ酸と違った光学特性を示します。
アミノ酸は世界的にほぼ統一された3文字で表現されています。
表1 アミノ酸の3文字表記
| グリシン | Gly | メチオニン | Met |
|---|---|---|---|
| アラニン | Ala | フェニルアラニン | Phe |
| バリン | Val | チロシン | Tyr |
| ロイシン | Leu | トリプトファン | Trp |
| イソロイシン | Ile | プロリン | Pro |
| グルタミン | Gln | アスパラギン酸 | Asp |
| アスパラギン | Asn | グルタミン酸 | Glu |
| セリン | Ser | リシン | Lys |
| スレオニン | Thr | アルギニン | Arg |
| システイン | Cys | ヒスチジン | His |
アミノ酸分析の分野では、伝統的にアスパラギン(Asn)はAspNH2、グルタミン(Gln)はGluNH2と表記される場合がありますので注意が必要です。同様にCysと表記した場合にはシスチンを指す場合があります。
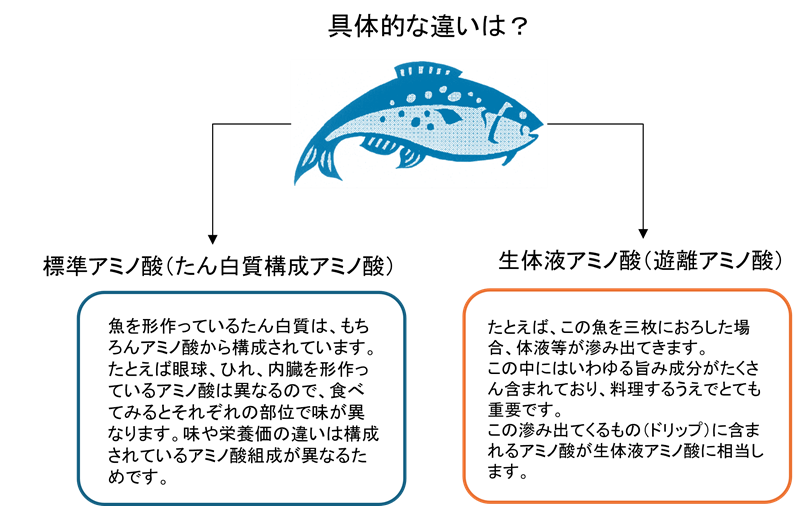
1) 標準アミノ酸(たん白質構成アミノ酸)
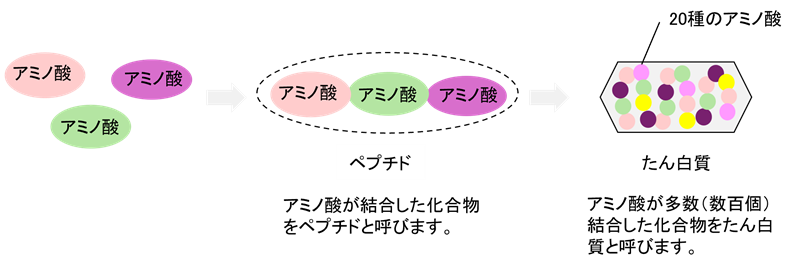
すべての動物を構成しているたん白質は、アミノ酸によって構成されています。たん白質を構成するアミノ酸を標準アミノ酸(たん白質構成アミノ酸)と呼びます。
標準アミノ酸は約20種と言われています。
2) 生体液アミノ酸(遊離アミノ酸)
アミノ酸の基本は、先の標準アミノ酸20種類ですが、その他にも単体で生体内や自然界に存在するアミノ酸が多くあります。それらのアミノ酸やアミノ酸代謝物、前駆体は生体液アミノ酸(遊離アミノ酸)と呼ばれています。
2. アミノ酸の分析方法
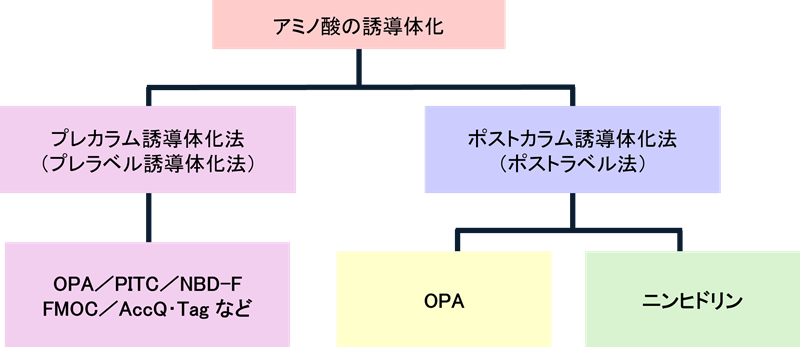
アミノ酸は親水性が高いこと、UV吸収や蛍光性を有するは少ないことから分離、検出が困難な物質の一つです。そのため、誘導体化(ラベル化)して検出する必要があります。誘導体化することでUV吸収や蛍光性などの化学的特徴を持った化合物となり分離、検出が可能になります。
アミノ酸の誘導体化には大きく分けてポストカラム/プレカラム誘導体化法の2種類の誘導体化法があり、使用する誘導体化試薬(ラベル化試薬)が異なります。
3. プレカラム誘導体化法とポストカラム誘導体化法の違い
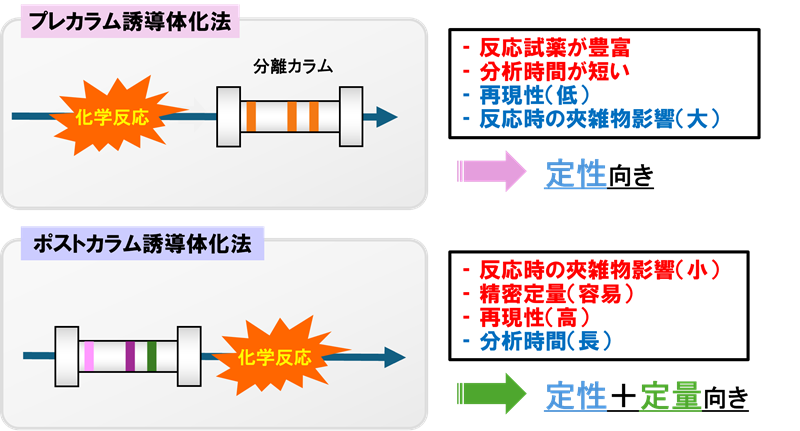
2つの誘導体化法には異なる特徴があります。アミノ酸成分をカラム分離する前に誘導体化するプレカラム誘導体化法は反応試薬の種類が多く比較的分析時間が短い反面、再現性が低く夾雑物の影響を受けるため定量より定性に向いています。一方、カラム分離後に誘導体化するポストカラム誘導体化法は夾雑物の影響が少なく再現性が高いことから、遊離アミノ酸を含む多くの成分の精密定量が可能です。
アミノ酸分析法の特徴についてまとめます。
表2 アミノ酸誘導体化法とその特徴
| 項目 | アミノ酸分析法 | ||
|---|---|---|---|
| 誘導体化法 | プレカラム誘導体化法 | ポストカラム誘導体化法 | |
| 反応試薬 | OPA/PITC/NBD-F FMOC/AccQ・Tag など |
OPA | ニンヒドリン |
| 特徴 |
- 試薬の種類(多) - 分析時間(短) - 夾雑物の影響(大) - 分離可能なアミノ酸の種類(少)※ - 再現性(低い)※ ※ポストカラム誘導体化法比 |
- 高感度 - 2級アミンは反応しない - 試薬や反応生成物の劣化が早い |
- 定量精度(高) - 夾雑物の影響(小) - 分離可能なアミノ酸の種類(多) - 分析時間(長) |
| 装置 | - 汎用LCシステム - 超高速LCシステム - LC-MS |
- 汎用LCシステム | - 高速アミノ酸分析計(専用機) - 汎用LCシステム |
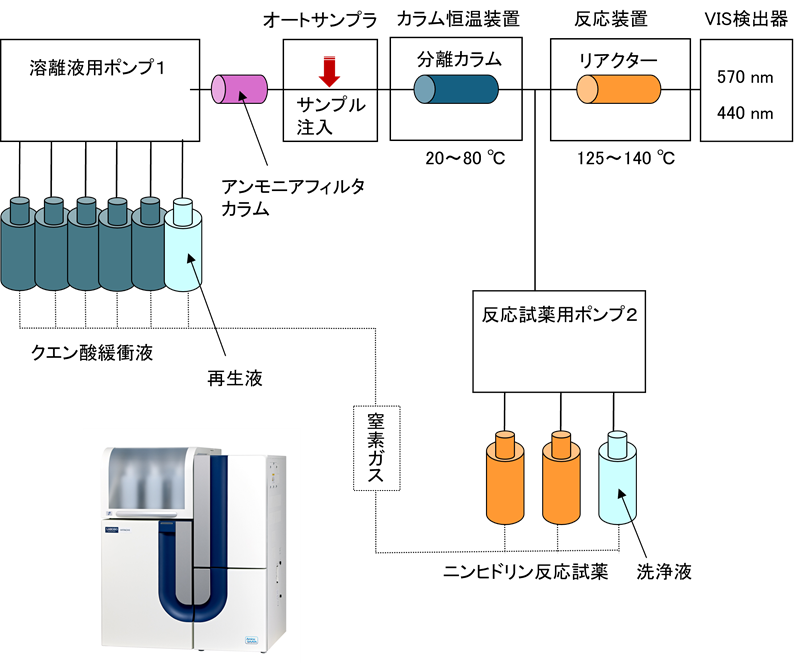
4. 日立高速アミノ酸分析計 LA8080 AminoSAAYA
日立高速アミノ酸分析計では、陽イオン交換カラムを使用したpHグラジエントによる分離と、ニンヒドリン試薬を使用したポストカラム誘導体化法を採用しており、定量精度及び再現性が良好です。
また、試薬の安定性も高く、40種類以上ののアミノ酸の一斉分析が可能です。
参考 陽イオン交換カラムとアミノ酸分離
- 酸性溶液中ではアミノ酸は+にチャージされることになり、陽イオン交換樹脂に対し、電気的な引力が生じます。
- 中性溶液中ではアミノ酸の分子中に+と-の電荷が生じ、陽イオン交換樹脂への引力が弱められます。
- アルカリ性溶液中では、アミノ酸は-にチャージされることにより、陽イオン交換樹脂に対し反発して素通りします。(これを利用して分析後のカラム洗浄には水酸化ナトリウム溶液等の高pH溶液を用い、残留するその他の成分を流し出します。これを再生(RG)と呼んでいます。)
- 以上のように、酸性→中性→塩基性へ溶離液のpHを変えていくことにより、段階的に各アミノ酸を溶出させ分離します。

陽イオン交換カラムはアルカリ洗浄が可能など化学的な強度が高い半面、物理的な強度は高くありません。圧力な急激な変動はカラム劣化の恐れがあるので、使用の際は注意が必要です。

表3 ポストカラム誘導体化法におけるアミノ酸分析用緩衝液に必要な要素
| 条件 | 使用する試薬 |
|---|---|
| pH | クエン酸 |
| イオン強度 | 塩化ナトリウム、塩化リチウム |
| 緩衝能 | クエン酸ナトリウム、クエン酸リチウム |
表4 ポストカラム誘導体化法におけるアミノ酸分析用緩衝液のその他成分と添加目的
| 試薬 | 目的 |
|---|---|
| エチルアルコール | Thr-Serの分離向上 |
| ベンジルアルコール | Trpの分離向上 |
| β-チオグリコール | 含硫アミノ酸の酸化防止 |
| Brij-35 | ポンプ圧力低減 |
| カプリル酸 | 腐敗防止 |
なお、日立高速アミノ酸分析計で用いる緩衝液およびニンヒドリン試薬は富士フイルム和光純薬株式会社よりMCI緩衝液PH/PFキットおよび日立用ニンヒドリン発色溶液キットとして販売されています。