Beyond Natural Antibodies?
- Novel Synthetic Antibodies Emerging from Molecular Imprinting -

神戸大学 大学院工学研究科 応用化学専攻
教授
竹内 俊文(薬学博士)
抗体は、抗原(標的分子)に対して高い選択性をもち、生体の防御をつかさどる免疫システムにおいて大きな役割を担う。この高選択的な抗原抗体反応は、各種酵素免疫測定法(ELISA)に活用され、病気の診断、食品分析、環境アセスメントなどに適用されている。最近は、抗体を用いた医薬品も開発され、がん細胞をピンポイントで狙い撃ちして高い治療効果を挙げている。
抗体は、高い性能をもつ反面、生体成分であるがゆえにその製造は容易ではなく、また、安定性にも問題がある。もし、人工高分子で抗体と同様の機能が再現できれば、容易に製造が可能な上に、高い安定性も実現できる。1950年ぐらいから、標的分子の鋳型を高分子に取ることで、抗体のような標的分子に対する分子認識能が発現するという発想の下、人工抗体を獲得しようとする挑戦が始まった。この挑戦は、1970年代後半に「分子インプリンティング」1, 2)として結実し、分子の鋳型を高分子内に取る技術として確立された。分子インプリンティングは、鋳型を取る分子(鋳型分子)と機能性モノマーの複合体を形成させ、架橋剤と共に共重合した後、鋳型分子を除去することで、鋳型分子に対して相補的な結合空間をもつ分子インプリントポリマー(MIP)を得る手法である(図1)。MIPは、簡便に合成できることから、抗体に代わる人工抗体として期待されているが、残念ながら、これまで報告されてきたMIPは、基本的には1970年代に確立された技術をもとに作製されていることから、分子認識能などの単一機能しかもたず、天然の抗体や酵素がもつ多様な機能にまったく及ばない。
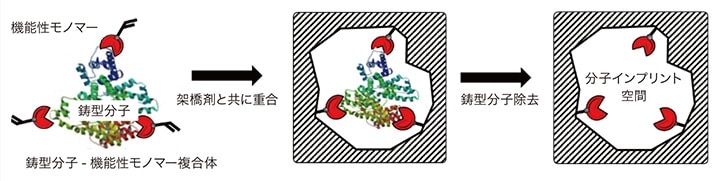
図1 分子インプリンティングの概念図
最近、著者らは、生体におけるタンパク質生合成の最終過程である翻訳後修飾を参考に、MIP作製後、そのインプリント空間内に部位特異的化学修飾を行うことで、MIPに機能の付与・変換・調整を行うことに成功し、これをポストインプリンティング修飾(PIM)と名付けた3-9)。本稿では、結合情報を蛍光変化に変換する機能をもつMIP4)を例に取り、PIMによって導かれる、天然抗体を超える勢いで発展しているMIPの新展開について概説する。
天然の抗体は、抗原に対して高い特異性と親和性を示し、ELISAなどの酵素免疫測定法に用いられている。ただし、東工大・上田らが報告している抗体断片Q-body10)を除けば、結合情報を可視化できる抗体は調製が困難で、捕捉抗体と検出抗体を併用したサンドイッチアッセイが主流である。このような洗浄と試薬添加を繰り返す手法では、迅速な定量は望めず、またリアルタイムモニタリングは不可能である。一方、MIPは、人工材料ゆえに、蛍光性の機能性モノマーを用いれば、蛍光性インプリントポリマーが調製可能で、結合挙動を蛍光測定によって検出可能である。ただし、MIPに蛍光分子の一部がランダムに配置されてしまうと、バックグランド蛍光が高くなり、検出感度が低下するなどの問題がある。
我々の開発したPIMで、MIPのインプリント空間のみに、相互作用部位や蛍光レポーター分子を部位特異的に導入することができれば、非特異的吸着が抑制される上に、インプリント空間に対する結合情報を、蛍光変化で読み出すことが可能となる(情報発信型MIPの創製)。分子インプリンティングの際、可逆結合をもつ機能性モノマーを標的タンパク質に共有結合で導入し、重合後、可逆結合を切断して標的タンパク質を除去すれば、インプリント空間内には、切断された可逆結合の片方の官能基が残る。この官能基は、原理的にインプリント空間内にしか存在しないことから、この空間内官能基に相互作用部位や蛍光レポーター分子を導入するPIMを施すことにより、MIPのインプリント空間のみに相互作用部位と蛍光レポーター分子を導入することができる。
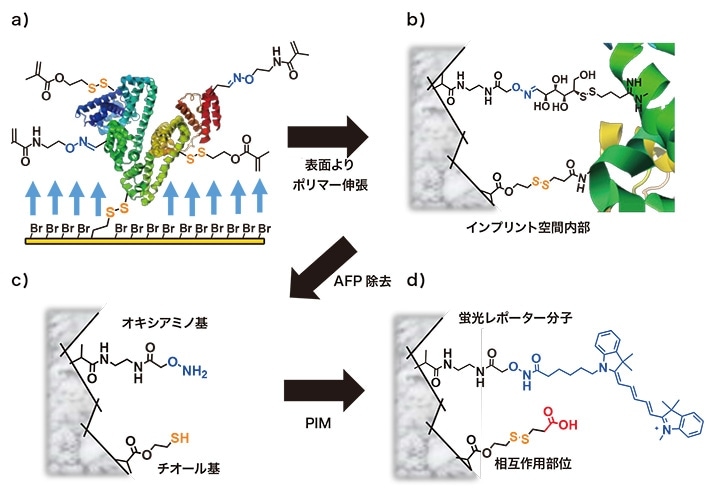
図2 AFPインプリント空間の形成とPIMによる相互作用部位と蛍光レポーター分子の導入4)
本稿では、PIMを利用したMIPによる、肝がんや肝疾患のバイオマーカータンパク質α-フェトプロテイン(AFP)の高感度・高選択的なセンシングを紹介する4)。まず、PIM可能な可逆結合(オキシム結合、ジスルフィド結合)を有する2種の機能性モノマーを新たに設計・合成し、これらを共有結合でAFP表面に導入したAFP複合体を、鋳型分子としてセンサ基板上に固定化し(図2a)、ポリマー膜厚を重合時間で調整可能な表面開始原子移動ラジカル重合により、基板上からポリマー薄膜を約10 nm成長させた(図2b)。ジスルフィド結合およびオキシム結合を切断してAFPをポリマー薄膜内から除去することで、AFPの形状にフィットするインプリント空間を形成した。この空間内には、ジスルフィド結合およびオキシム結合を切断した後の遊離のチオール基とオキシアミノ基が残存する(図2c)。ここで強調したいことは、この2種類の官能基は、AFPに共有結合されたままポリマー内に導入された可逆結合由来であることから、原理的に、インプリント空間のみにしか存在しない。従って、インプリント空間の形成後に行うPIMは、空間内選択的な修飾となる。今回は、チオール基にはAFPに対する相互作用基(カルボキシ基)、オキシアミノ基には蛍光レポーター分子(Cy5)を導入した(図2d)。これにより、相互作用部位や蛍光レポーター分子がインプリント空間のみに配置され、非特異的吸着やバックグランド蛍光による感度の低下が防止できることから、高感度かつ高選択的にAFPを認識・検出可能なMIPが合成可能となる。
実際、同じMIPを成膜したセンサチップを用いて、高感度バイオセンサとして汎用されている表面プラズモン共鳴センサBIACORE 3000と、蛍光顕微鏡によるセンシングの検出限界を比較してみた。その結果、BIACORE 3000では20 ng/mL(280 fM)であった一方、蛍光センシングでは1 ng/mL(14 fM)と、同じMIP薄膜を用いているにもかかわらず、検出限界が20倍向上し、市販のELISAと遜色ない検出感度を達成した。これは、BIACORE 3000は、MIPに結合する物質すべてを検出してしまうが、蛍光センシングでは、PIMによりインプリント空間のみに蛍光を導入しているので、インプリント空間に対するAFPの結合を、より選択的に検出した結果といえる。また、ヒト血清アルブミンや前立腺特異抗原(前立腺がんのバイオマーカー)はほとんど検出されず、高い選択性をもつことも実証した。PIMの効果を確かめるため、インプリント空間内のチオール基に、相互作用基(カルボキシ基)に代えてヒドロキシ基を導入したところ、蛍光変化はほとんど観察されず、確かにPIMの足場となる空間内にはチオール基が残存し、PIMにより、AFPとの結合に都合のよいチオール基の位置に、AFPと相互作用するカルボキシ基が導入されていることが明らかとなった。
以上示したように、可逆結合をもつ複数の機能性モノマーを用いた分子インプリンティングと多段階PIMにより、標的タンパク質に対して、優れた結合親和性と検出感度を有する人工抗体が構築可能であった。また、その検出感度はELISAに匹敵し、臨床応用可能なほど良好であった。このMIPによる蛍光センシングは、試薬添加など煩雑な操作が必要ないのも特徴で、操作性は圧倒的にELISAに勝る。また、PIMにより、部位特異的な官能基変換が容易にできることから、相互作用基および蛍光レポーター分子のインプリント空間内でのin-cavityスクリーニングも可能となり、高感度・高選択的検出を達成するための最適化を行うことにより、更なる高感度・高選択的な人工抗体が得られる。最近、MIPナノ粒子によるドラッグデリバリーシステムも報告しており11)、分子インプリンティングは、画期的な手法に変貌しつつある。ライフサイエンスやバイオテクノロジーなど抗体を多用する分野に対して、大きな影響と波及効果を与えつつあり、MIPも含めた生体機能性人工材料研究において、抗体を超えることは、ある意味夢のような達成目標であったが、Beyond Natural Antibodiesが、そろそろ視野に入り始めたことを強調したい。乞うご期待である。
参考文献
さらに表示