The application of fluorescence fingerprint measurement with F-7100 to the natural product researches

近畿大学農学部水産学科
水産利用学教室
准教授
福田 隆志 博士(農学)
微生物を資源とした創薬研究は、1928年のアレクサンダー・フレミングによる青カビからのペニシリンの発見とその後の実用化により、大きく発展した。その過程で、抗生物質のストレプトマイシンやエリスロマイシン、抗真菌剤ではアンホテリシンB、抗がん剤ではマイトマイシンやアドリアマイシン、さらには免疫抑制剤のタクロシムスといった、今まさに臨床で用いられている医薬品が微生物より発見された。それら医薬品の中でも最も我々の記憶に新しいのは、2015年大村智博士のノーベル生理学・医学賞の受賞理由にもなったエバーメクチンである1)。エバーメクチンは、放線菌Streptomyces avermitilisが生産する二次代謝産物であり、抗寄生虫薬として多くのアフリカ住民を失明の危険から救った。本受賞は、大村先生の功績を讃えるのみならず、微生物からの天然物創薬研究の重要性を再認識させるものでもあった。
一方で最近の天然物創薬研究の興味は、陸上から海洋へとその対象を変化させている。海洋には10億種以上の微生物が生育していると推測されているが、その90%以上が未知であると推定されている。このことから、海洋由来微生物は創薬研究の材料として大きなポテンシャルを有していると考えられている。例えばpinabulin2)やmarizomib3)は海洋微生物が生産する化合物であり、現在米国で抗がん剤としての臨床試験が進められている。また申請者がやはり海洋微生物培養液中より発見したメラノーマ選択的な抗がん活性を示すseriniquinone A4)は、現在米国の製薬会社に注目されている。
このように海洋由来微生物は創薬資源として現在非常に注目を浴びているが、常に我々天然物研究者の頭を悩ませているのが、いかに早い段階で有用な物質生産を行う菌株を選択するか、または今までに報告例の無い新規化合物を生産する菌株(他とは異なった物質生産能を有する菌株)を選択するか、である。この悩みを解決するため、研究者は日々様々な努力、検討を行っている。例えば、難培養性菌や生物共生菌の培養条件検討、通常は眠っている生合成遺伝子を起こす培養条件検討、遺伝子を改変させて新規物質生産を促す検討、さらには遺伝子そのものを環境中より取得しホストとなる微生物で異種発現させる手法などが挙げられる。しかし、何れの場合もその後に二次代謝産物の生産条件の検討を行う必要があり、新規有用物質発見の近道とは言い難い。やはり確実なのは、従来通り分離できた菌を培養し、その二次代謝産物を様々な分析・比較をすることで、その中から特徴的な培養液を選択することが一番だと考えられる。
培養液中に含まれる二次代謝産物の分析方法としては、液体クロマトグラフィーに紫外可視吸光光度検出器(LC-UV)を用いたUV吸収による網羅的な代謝物の分析、液体クロマトグラフィーに質量検出器(LC-MS)を用いた分子量による網羅的な代謝物の分析、さらにはLC-MS/MSを用いたモレキュラーネットワーキング5)の手法などが用いられている。しかし、これら手法はいずれも高速液体クロマトグラフィー(HPLC)を用いて化合物を分離する必要があるため、1サンプルの解析に多少なりとも時間を有する。もし分離の必要がない培養液のままでの分析ができ、それら個々の培養液の特徴を可視化(数値化)する手法があれば、理想である。そこで今回は、微生物培養液に含まれる蛍光物質に着目した。
蛍光物質とは、吸収した光エネルギーを蛍光として放出する特徴を有した化合物群である。このような特徴を有する化合物には、構造中にベンゼン環やトリアゾール環を含むものが知られており、工業的には染料、顔料、インク、研究試薬などに利用されている。これら化合物群の検出には、励起波長の光を照射し、放出された蛍光波長を測定することで行う。そのため微生物培養液のような複数の化合物の混合液でも、蛍光物質のみの網羅的な検出が可能と考えられる。すなわち本研究は、蛍光物質を利用した特徴ある微生物培養液の簡便な選択方法の提案である。
実験に使用した菌の分離は、東シナ海、瀬戸内海および種子島の海洋環境より採取した土壌サンプルおよび海洋生物サンプルから行った。
滅菌水で希釈したサンプルの上清(100 µL)を天然海水のみの寒天培地に塗布し、27℃の条件で培養を行った。4週間後シャーレ内に現れたコロニーを釣菌することで、海洋由来放線菌およびバクテリア(48サンプル)を分離した。
菌の培養はM1(+)培地(天然海水使用)とM1(−)培地(蒸留水使用)の2種の培地条件で行った。M1(+)培地はSoluble starch(1.0%)、Bacto™ Yeast extract(0.4%)、Bacto™ Peptone(0.2%)、CaCO3(0.1%)、KBr(0.01%)、Fe2(SO4)3・7H2O(0.004%)を天然海水(1 L)で溶解した。M1(−)培地はM1(+)培地の天然海水を蒸留水に置き換えたものとした。
各培地を100 µL三角フラスコにそれぞれ25 µL加え綿栓後、121℃、15分間滅菌処理を行った。培地を室温に戻し、純培養を行った48種の菌(菌株番号153~200)をそれぞれ1白金耳ずつ植菌し、生産培養を行った。生産培養は27℃、160 rpmの条件で行った。14日間培養後、25 µLのエタールを加え1時間振とうすることで微生物抽出液とした。(計96サンプル)
微生物抽出液の上澄み(1 mL)をエッペンチューブに移し、10,000 rpmで15分遠心後、上清300 µLを蛍光測定用96 wellプレートに移し、測定サンプルとした。
測定は図1に示す機器を用いて、200~600 nmの励起波長に対し200~600 nmの蛍光波長を網羅的に測定する三次元蛍光スペクトル(蛍光指紋)を取得した。
使用機種
F-7100形分光蛍光光度計

図1 測定に使用した機器
菌株番号153(−)、153(+)、171(−)、171(+)、188(−)、188(+)、190(−)、191(−)、193(−)、194(−)の培養液で、蛍光波長390~400 nmの波長範囲において強い蛍光を確認した。そのデータを図2に示す。
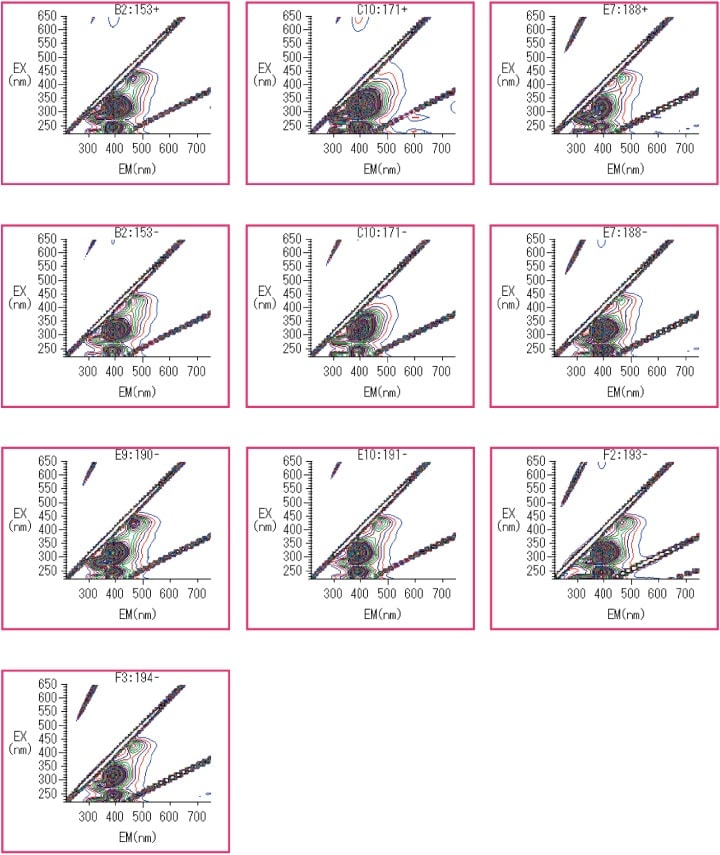
図2 蛍光波長:390~400 nmで強い蛍光が見られた培養液
菌株番号175(+)、176(+)、177(−)、177(+)、180(−)の培養液で、蛍光波長430 nm以上の波長範囲において強い蛍光を確認した。そのデータを図3に示す。
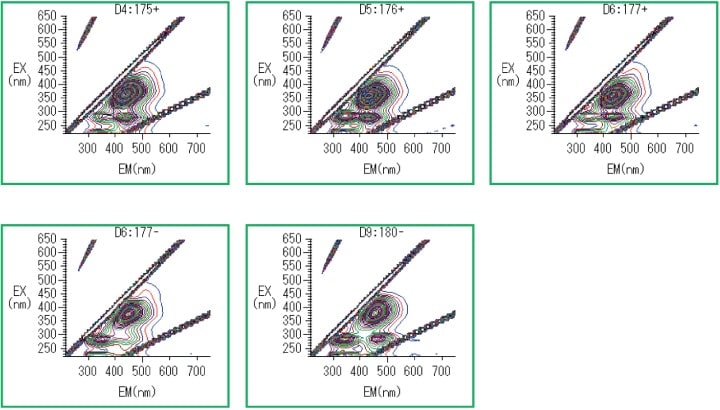
図3 蛍光波長:430 nm以上で強い蛍光が見られた培養液
測定結果をもとに、ピークトップおよびピークバレーに相当する特徴的な13波長選択し(図4)、多変量解析ソフトJMP12.2を用いて主成分分析を行った。
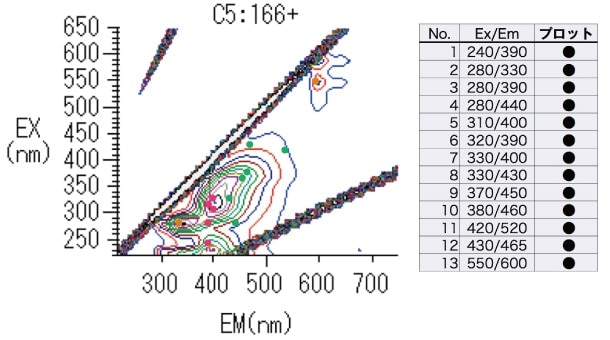
図4 選択した13波長
その結果を図5示す。多くの培養液は中心部にプロットされたが、390~400 nmで強い蛍光が見られた培養液は右下部にプロット(赤枠内)された。また、430 nm以上で強い蛍光が見られた培養液は右上部に一群としてプロット(緑枠内)された。
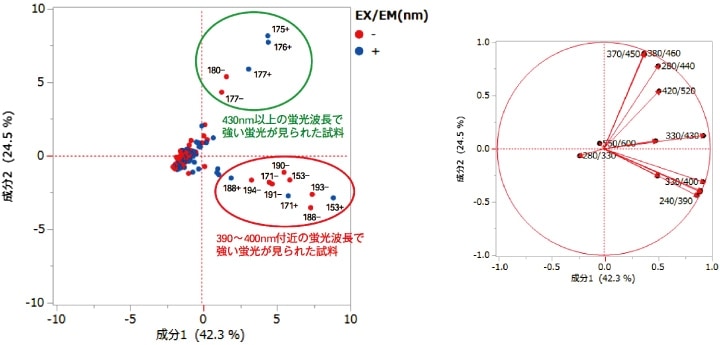
図5 多変量解析結果
今回我々は、特徴的な海洋微生物の培養液を選択する一つの方法として、蛍光指紋を利用した多変量解析を試みた。本方法を用いることで、特徴的な2つのグループを見出すことに成功した(図5)。菌株171および188は、培地中の海水の有無にかかわらず390~400 nmの蛍光波長で強い蛍光物質の産生が確認され、同様に菌株177でも培地中の海水の有無にかかわらず430 nm以上の蛍光波長で強い蛍光物質の産生が確認された。この結果は、それぞれの蛍光物質がそれぞれの菌を特徴付ける化合物である可能性が考えられ、非常に興味深い。
また海水の有無による蛍光物質の生産に対する影響に着目すると、蛍光波長:390~400 nmで強い蛍光が見られた10培養液中、7つが海水非添加の生産培地であった。逆に蛍光波長:430 nm以上で強い蛍光が見られた5培養液では3つが海水添加培地であった。まだサンプル数が少ないため断言はできないが、海水添加培地でより高波長側で蛍光を発する化合物の生産が促されている可能性が示唆された。
現在蛍光指紋は、食品科学の分野で品質評価(異物の混入や生産地の判定)に用いられている。本手法は、食品のような多数の化合物が混在したサンプルでも蛍光物質を網羅的に計測することが可能であること、ごく簡単な必要最低限の前処理で測定が可能であること、さらには得られる情報が膨大で網羅的解析が可能であることから、食品の一次スクリーニング(有害物質の検出)としての応用も期待されている6)。
今回この蛍光指紋の考え方を微生物培養液の選択に応用し、特徴的な蛍光物質生産を行う菌株を迅速に選択することに成功した。今後、本手法が新規有用物質発見の強力な手助けになることを期待する。また、従来のLC-UVやLC-MSを用いた分析結果と情報を共有させることで、さらに精度の高い有用菌株の選択が可能になると期待されるため、現在共同研究者と共に分析を進めている。この成果については続報を待たれたい。
最後に、「なぜ暗い海底に生きる海洋微生物が、蛍光物質を生産する能力を有しているのか?」この謎の答えもこれら微生物を調べることで、明らかにしたい。
謝辞
今回紹介した研究は、北里大学薬学部供田洋教授のもとで行われました。また東シナ海の海洋サンプルは、東京海洋大学今田千秋教授よりご提供いただきました。また本資料を作成するにあたり、東北医科薬科大学薬学部内田龍児教授にご協力及びご助言をいただきました。この場を借りて深く感謝いたします。
参考文献
さらに表示