Effect of Alcohol Content on the Ionomer Adsorption of Polymer Electrolyte Membrane Fuel Cell Catalysts

九州大学大学院工学研究院
教授
藤ヶ谷 剛彦 博士(工学)
固体高分子形燃料電池(PEMFC)は、水素をエネルギー源とすることから持続可能な低炭素社会の実現に向けた重要な電源として期待されている1,2)。さらなる普及に向けて、PEMFCのコスト削減は重要な課題であるが、特にコスト削減効果が大きい触媒層に含まれる白金量の削減技術の確立が急務である。そのためにまずできることは白金(Pt)の利用効率向上であり、多くの研究が展開されている2-5)。触媒層は一般的に白金ナノ粒子が担持されたカーボン(Pt/C)とプロトン伝導性のポリマー(アイオノマー)からなる3次元多孔質構造である6)。アノードで生成されたプロトンと電子が外部から供給される酸素ガスと白金ナノ粒子上で反応して水を生成するカソード触媒層の酸素還元反応(ORR)が電池反応の律速反応である。触媒層内のアイオノマー分布と空孔の接続性がプロトン拡散と酸素拡散を支配し、これらの拡散がORRの過電圧を生じることから、特にカソード触媒層の構造制御が重要とされる7)。このようなプロトンと酸素の拡散を有利にするような構造の作製に、Pt/Cとアイオノマーと分散溶剤からなる溶液(=「インク」と呼ぶ)の組成や作製法の最適化が重要であり8)標準化のために推奨されたプロトコルもあるものの、各研究グループ、各メーカーによって秘伝の条件が存在する(はず)。
インク組成の中でもアイオノマーの相対量(炭素対イオノマーの重量比= I/C)は制御が容易であることから、しばしば最適化の対象となる9-18)。一般的にはI/Cを小さくすると酸素拡散性が向上する一方で、プロトン伝導ネットワークの切断によりプロトン伝導度が低下するトレードオフの傾向を示す10)。また、インク溶媒の種類もPEMFCの性能に影響を与えることが知られ、特に、メタノール、エタノール、2-プロパノールなどのアルコールと水の二元混合溶媒を中心に広く研究されている19-31)。
アルコール/水の混合比を制御したいくつかの研究を紹介しよう。Van Cleve らは、水分率が高い(水分率83 wt%)インク中では、Ptとアイオノマー中のスルホン酸との強い相互作用が働き、結果としてORR活性の低下を招く一方で、低水分率(24 wt%)のインクでは大きなアイオノマー凝集体が生成し、触媒層において酸素拡散の妨げとなり、結局、中程度の水分率(62 wt%)のインク溶媒を使用した場合においてPEMFC性能が最も優れることを報告した30)。一方でOrfanidiらは、水分率の多い(65 wt%)インクの方が水分率の少ない(16 wt%)インクより性能が低いとする逆の結果を報告した。彼らの考察によると、高水分率インク中で形成されるアイオノマー凝集体が触媒層中において空孔を閉塞し、酸素拡散を妨げた一方、低水分率(高アルコール分率)条件下では、アイオノマーはより均一に分布し、Pt表面での連続的なプロトン伝導パスが形成された結果、良好な性能を与えたとしている29)。これらの研究から、インク中のアイオノマー、溶媒分子、およびカーボン表面との相互作用が、触媒層内でのアイオノマー分布や空孔構造の連続性を制御する上で重要であることを示している。しかし、溶媒組成に応じた触媒に対するアイオノマー吸着の体系的かつ定量的な分析はまだ行われていなかった。
そこで我々は、高水分率(80 wt%:「水リッチ溶媒」と呼称)および低水分率(13 wt%:「アルコールリッチ溶媒」と呼称)の2種類のエタノール水溶液インク中でのカーボン担体およびPt/Cへのアイオノマーの吸着挙動を吸着等温解析により評価した。また、それぞれのインクから作成した触媒層を組み込んだ燃料電池セルを作成し、電池性能との比較も行った。
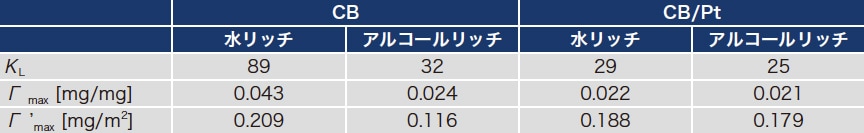
アイオノマーとしては最も広く使用され、優れたプロトン伝導性を持つPFSA(フッ素化ポリエチレンベースのポリマー)であるナフィオンを用い32)、カーボンとしてはこちらも汎用のVulcan(CB)を用いた。図1a は水リッチ溶媒(青線)およびアルコールリッチ溶媒(黒線)におけるナフィオンのCBへの吸着挙動を示す吸着等温線である。ナフィオンの吸着量の定量は重量法33)、密度測定34)、と比較し定量性の高い19F-NMRにより行った。本研究はアルコール/ 水混合溶液で行ったが、水単一溶媒でのナフィオンの吸着等温測定は19F-NMRを用いて報告されている35-37)。ナフィオンの平衡濃度(Ce)に対してプロットしている2種類(水リッチ・アルコールリッチ)の溶媒いずれの場合においても2段階の吸着プロファイルが観察され、水単一溶媒の際35-38)と同様に多層吸着が示唆された。CB表面の化学構造は均一ではなく、理論的にはこのような不均一な表面への吸着はラングミュアモデルに従わないはずであるが、ラングミュア式を適用した際のフィッティングのR2値は0.95以上であり、有意な解析であると判断した。ラングミュア式を用いたフィッティングから、ナフィオンのCBへの第一層吸着の平衡吸着定数(KL)を求めたところ水リッチ溶媒でKL=89とアルコールリッチ溶媒のKL=32より大きく、水リッチ溶媒中ではより強く相互作用することが明らかとなった。さらに、第一層目吸着の最大吸着量(Γmax)は、水リッチ溶媒でΓmax=0.043 mg/mgとアルコールリッチ溶媒中でのΓmax=0.024 mg/mg より大きく、水リッチ溶媒は相互作用のみならず吸着量においても有利であった(表1)。水リッチ溶媒中では、疎水性のCF2主鎖が疎水性相互作用によりCB表面に優先的に吸着している一方、アルコールリッチ溶媒では、ナフィオンはアルコール分子により溶媒和しているため、吸着が有利に進行しないと考えられる。興味深いことに、水リッチ溶媒における第一層吸着はCe= 約 0.04 mg/mL付近から始まるのに対し、アルコールリッチ溶媒の場合においてはより低濃度のCe= 約 0.02 mg/mL付近から立ち上がっている。ナフィオンは、CF2主鎖間の強い疎水性相互作用により、水リッチ溶媒中でバンドルを形成する一方で、アルコールリッチ溶媒中では、アルコール分子によるCF2主鎖への溶媒和により、孤立分散に近いことが知られており39-40)、水リッチ溶媒では見かけの濃度が下がっているために、このような逆転現象が起こっていると考えている。吸着等温測定だけでも様々な効果が垣間見えて興味深い。このような、ナフィオンのバンドル形成も加味すると、水リッチ溶媒中で見られたより大きなΓmaxには、吸着力の強さ以外にもバンドル形成の効果も含まれているだろう。
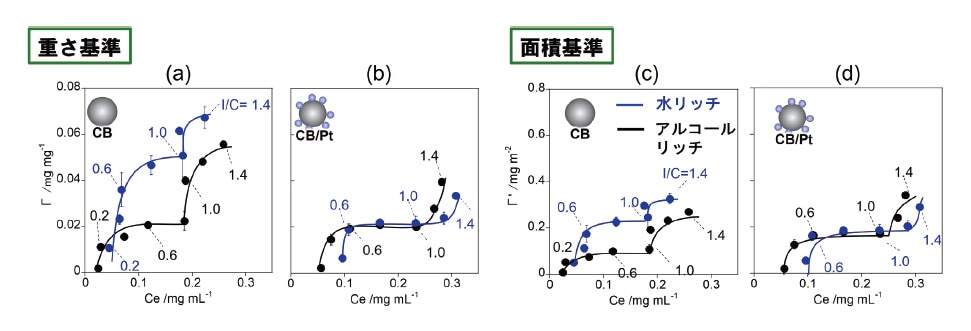
図1 (a, c)CBに対するナフィオンの吸着等温曲線および(b, d)CB/Ptに対するナフィオンの吸着等温曲線。(a, b)重量および(c, d)比表面積で規格化した水リッチ(青線)ならびにアルコールリッチ(黒線)の等温吸着曲線
表1 CBおよびCB/Ptに対するナフィオン吸着のKL、Γmax、およびΓ'max
また、同様のナフィオン吸着挙動の解析をPt担持CB(CB/Pt、白金担持率46 wt%)に対しても行った(図1b)。水リッチおよびアルコールリッチ溶媒におけるKL はそれぞれKL=29とKL=25と、CBに対するKLより大幅に小さかった(表1)。この結果は、アルコール含有量に関係なく、Pt表面に対するナフィオンの相互作用がCB表面への相互作用よりも小さいことを示唆している38)。一方、CB/Ptに対するΓmax(mg/mg)は、CBに対する値と比較し、水リッチ溶媒において特に減少した(図1b)。白金という重い原子を含むことによる過小評価があることも考慮し、重量当たりではなく表面積当たりのナフィオン吸着量を比較するため、窒素吸着測定から算出したBET表面積(m2/g)で規格化した新たな指標Γ(' mg/m2)を定義し、改めてΓ'を用いて比較したところ、水リッチ溶媒においてCBではΓ'max=0.209 mg/m2、CB/PtではΓ'max=0.188 mg/m2と傾向は変わらなかった。従って、ナフィオンは水リッチ溶媒中においてはPt表面よりもCB表面に優先的に吸着すると考えている。一方、アルコールリッチ条件では、CB/PtにおいてΓ'max=0.179 mg/m2とCBの時のΓ'max=0.116 mg/m2よりも大きく、ナフィオンはアルコールリッチ溶媒中ではPt表面に優先的に吸着することを示唆する結果が得られた。
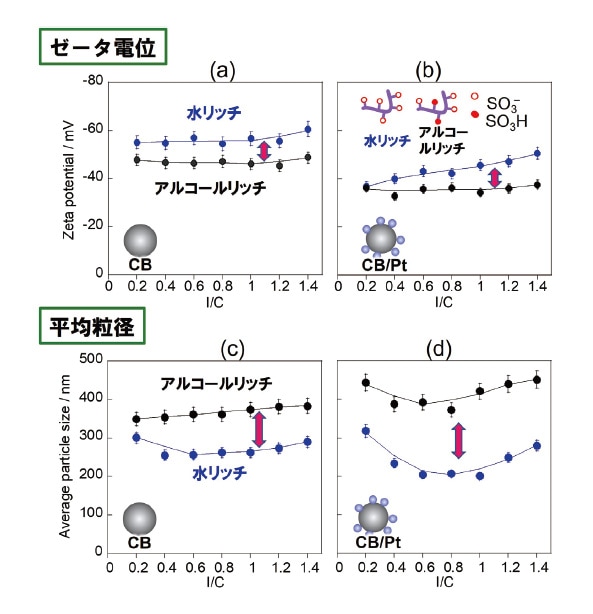
図2 水リッチ(青線)ならびにアルコールリッチ(黒線)溶媒における(a)CBおよび(b)CB/Ptのゼータ電位。水リッチ(青線)ならびにアルコールリッチ(黒線)溶媒における(c)CBおよび(d)CB/Ptの平均粒径。
上記の等温吸着測定において、I/Cの増加に伴いナフィオンの吸着量が増加することが明らかになったが、このような変化がCBまたはCB/Ptの分散性にどのように影響するかを調べるために、吸着等温実験と同じインクを用いてゼータ電位、粒径分布および、分散安定性を調べた。ナフィオンが存在しない場合(I/C = 0)、粒子の凝集と沈降が即座に起こるため、ゼータ電位や粒径の測定は困難であった。分散に対するナフィオンの役割が明確に理解できる。一方、図2a,bに示すようにI/C > 0.2ではゼータ電位は負であり、イオン化して負電荷をもつスルホン酸基の効果より安定したコロイド分散が得られたことを明確に示している。ゼータ電位の値はI/C 値に依存せずほぼ一定であった。これは、CBまたはCB/Pt表面では表面吸着したナフィオンとそれを緩く囲むナフィオン層が存在し、吸着等温測定では吸着ナフィオンのみが推定されたのに対し、ゼータ電位測定ではそれより外側まで囲む弱吸着性のナフィオン層表面を捉えていると考えている。ゼータ電位の絶対値が水リッチ溶媒においてより大きいのは、より大きな誘電率によりスルホン酸基のイオン化が進行していることを反映している21)。一方、CB/Ptのゼータ電位の絶対値は、いずれの溶媒においてもCBの絶対値より小さかった(図 2b)。Ptの存在下では、スルホン酸基がPt表面と相互作用し、正味の負電荷が減少したと考察している。
また、同じインクを用いて動的光散乱測定により水リッチ溶媒(青色)およびアルコールリッチ溶媒(黒色)中のCB(図2c)およびCB/Pt(図2d)の平均粒径を測定した。CBおよびCB/Ptでは、水リッチ溶媒において平均粒径サイズがより小さく、さらに直径分布がより狭いことが分かった。これは、水リッチ溶媒中ではナフィオンの吸着が強く、さらにスルホン酸のイオン化が進行しているために帯電量が大きく、粒子の分散性が高いことに起因している。一方、アルコールリッチ溶媒では、特にCB/Ptで1.0 μm を超える大きな粒子が存在するなど、分散性は劣っていた。インクの沈降実験により14 日間にわたり分散安定性を観察したところ、CB/Ptインクの水リッチ溶媒においては安定に分散状態を維持したのに対し(図3左)、アルコールリッチ溶媒では凝集が大きく、沈降が観察された(図3右)。水リッチ溶媒ではナフィオンの吸着とスルホン酸基のイオン化の効果で安定分散の目安とされる50 mV41に迫る大きなゼータ電位の絶対値であった一方、アルコールリッチ溶媒中ではスルホン酸基のイオン化とアイオノマーの吸着量は十分でなく、そのためにゼータ電位の絶対値が小さく、結果として凝集を引き起したのであろう(図4)。
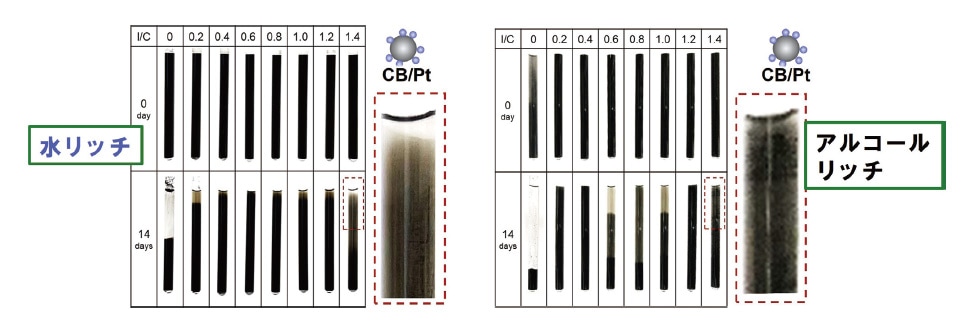
図3 (左)水リッチ溶媒と(右)アルコールリッチ溶媒におけるCB/Ptインクの沈降実験の様子
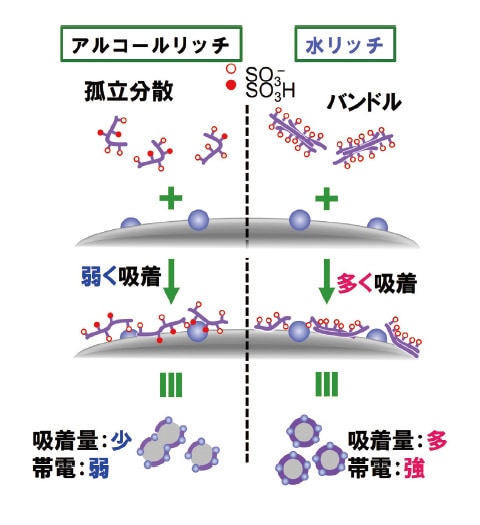
図4 (左)アルコールリッチ溶媒と(右)水リッチ溶媒におけるCB/Ptに対するナフィオン吸着挙動
表2 触媒層表面のゼータ電位
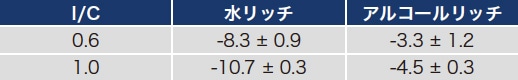
インク中での触媒表面スルホン酸基の量とイオン化状態が実際の触媒層にどのように反映するか調べるために、水リッチ溶媒とアルコールリッチ溶媒のインク(I/C = 0.6 および 1.0)をPET基板上に塗布し、触媒層表面のデータ電位を測定した。I/C = 0.6 および 1.0 の水リッチ溶媒からスプレーされた触媒層の表面ゼータ電位は、それぞれ‒8.3 mV および‒10.7 mV であったのに対し、アルコールリッチ溶媒から塗布した場合、それぞれ‒3.3 mVと ‒4.5 mV であった(表2)。これらのゼータ電位測定は全て水溶媒で行っていることからスルホン酸基のイオン化状態には差はなく、得られた差は触媒層表面に存在するスルホン酸基の数を反映している。すなわち、水リッチ溶媒から調製された触媒層表面ではアイオノマー量がより多いことが明らかとなった。水リッチ溶媒ではアイオノマーが触媒表面に強く吸着して乾燥後も表面にとどまったのに対し、アルコールリッチ溶媒では表面吸着が弱く、スルホン酸の残存が少ないと考えている。それでは、アルコールリッチ溶媒においては、アイオノマーはどこに行ったのだろうか? おそらくより毛管力により深い側に溜まり、乾燥後はCB/Pt凝集間の空孔を閉塞していると予想している。
水リッチ溶媒とアルコールリッチ溶媒で見られたナフィオン吸着挙動の違いがPEMFCの性能にどのように影響するかを調べるため、それぞれのインク(固体分率6 wt%)を塗布した電極触媒層(白金目付量0.3 mg/cm2)を含む2種類の膜電極接合体(MEA)を作成した。水リッチ溶媒から作成したMEAをw-MEA、アルコールリッチ溶媒から作成したMEAをa-MEAとし、インクにはナフィオンの第一層吸着濃度領域であるI/C = 0.72を選択した42)。触媒層表面の走査型電子顕微鏡(SEM)画像を図5a~fに示した(SU9000にて撮像)。まず、いずれの溶媒条件においても触媒層表面に大きなクラック構造は観察されず均一な構造であった。興味深いことに、w-MEAにおいては直径1~2 µm程度のボイド構造が均一に分布する様子が低倍率観察において確認できた(図5a、b)。このマイクロサイズのボイド構造は、水滴がテンプレートとして生じたと考えている26)。一方、a-MEAにはそのような構造は観察されていない。

図5 (a ~ c)w-MEAおよび(d ~ f)a-MEAの触媒層表面SEM写真。(a, d)1,300倍、(b, e)20,000倍、(c, f)300,000倍。
図6a にはアノードに水素、カソードに空気を供給した際のw-MEAとa-MEAの分極(I-V)曲線を示した(80℃、相対湿度100%)。青線で示したw-MEAは、全ての電流密度領域において黒線で示したa-MEAより高い起電力を示し、最大出力密度はw-MEAで750 mW/cm2、a-MEAで580 mW/cm2であった。MEAを用いた交流インピーダンス解析から求めた、w-MEAのプロトン抵抗は0.35 Ω /cmと、a-MEAの1.26 Ω /cm より小さいことが分かり、高い活性の理由の一つはw-MEAの触媒層においてプロトン拡散に有利な構造が構築されているためであることが明らかとなった。図6b には、w-MEAとa-MEAのカソードに窒素、アノードにH2を流して測定したサイクリックボルタモグラムを示した。0.1 ~ 0.3 Vに明確に観察された水素吸脱着ピークから電気化学的活性表面積(ECSA)を評価し、電気化学的にアクセス可能なPt表面積を求めたところ、w-MEAとa-MEAでそれぞれ 75.1 m2/gPtおよび 49.3 m2/gPtであった。w-MEAの方がプロトン拡散に有利で、さらにECSAが大きいことは、アイオノマーネットワークがよく発達し、Pt表面へのプロトンの送達を促進する構造が形成されているためと考えられる。吸着等温実験等から明らかになったように、水リッチ溶媒ではCB/Pt表面へのナフィオン吸着が有利で、結果的にプロトン伝導パスの発達につながったのであろう(図7左)。一方、アルコールリッチ溶媒中ではナフィオンはCB/Ptに吸着しづらく、インクの塗布時に空孔中に凝集したことで、アイオノマーネットワークは不均一化し、結果的にプロトン拡散抵抗の増大とECSAの低下へとつながったと考えている(図7右)20-21, 43)。
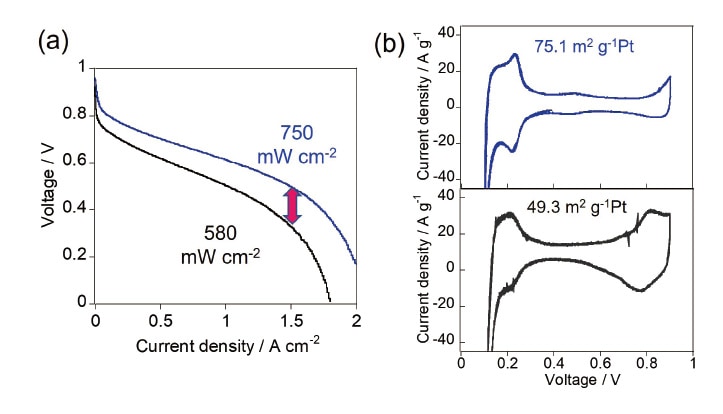
図6 w-MEA(青線)とa-MEA(黒線)の(a)分極曲線および(b)in-situ CV
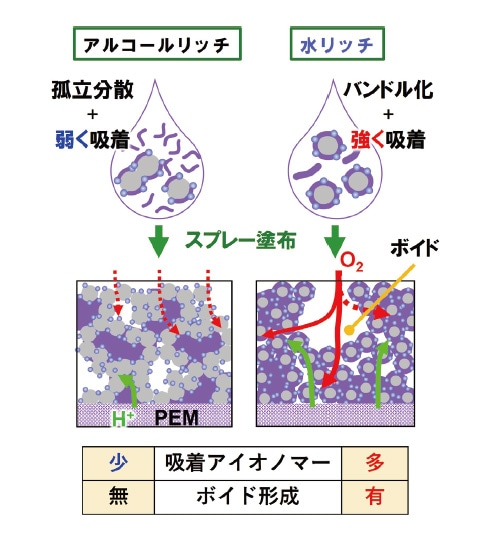
図7 (左)アルコールリッチ溶媒と(右)水リッチ溶媒からの触媒層形成挙動
カソードでの酸素還元反応(ORR)では、プロトンの拡散だけでなく、酸素拡散抵抗も関与しており、酸素拡散にはPt表面に吸着したアイオノマー中の拡散と、触媒層内のバルク空間での拡散の両方が影響することが知られている。MEAを用いた交流インピーダンスの解析結果から、w-MEAの方が酸素拡散抵抗も小さいことが明らかとなっている。アルコールリッチ溶媒では、アイオノマーの触媒表面への吸着力が小さいために、触媒層内のバルク空間に溜まることでバルク中の酸素拡散の抵抗になった一方(図7左)、水リッチ溶媒では触媒表面へアイオノマーが強く吸着し、バルクの空孔は保持され、さらにその細孔同士がマイクロボイドで接続されており、バルクの酸素拡散に有利な構造を形成したと考えられる(図7右)。Pt表面上に吸着したアイオノマーは、Pt表面への酸素分子の吸着を抑制することでORRを阻害することも知られているため、重要なファクターである26,44,45)。吸着等温測定で得られた結果からは、水リッチ溶媒中ではアイオノマーはPt表面よりカーボン表面への吸着が有利で、アルコールリッチ溶媒においてはPt表面への吸着が有利であった。しかし、これはインク中における吸着を捉えて考察したに過ぎず、過剰のアイオノマーが存在し、さらに乾燥過程という非平衡な状態を経る中での実際の吸着状態にどのように反映しているかに関しては、触媒層の電気化学的な解析など、より詳細な解析で明らかにしていきたい。
等温吸着測定から燃料電池インクの溶媒組成の違いによりアイオノマーの吸着状態が異なることを突き止め、水の割合が多い際はアイオノマー吸着が有利になることで、プロトン伝導パスが形成され、酸素拡散パスの確保にも有利に働くメカニズムを明らかにできた。触媒層表面に対するアイオノマーの吸着を制御することができれば、燃料電池性能を制御できる可能性を示しており、燃料電池性能の制御に対して新しい方法論を示したと言える46)。
参考文献
登録記事数 203件
まだまだあります。