Visualization of the Photodegradation of a Therapeutic Drug by EEM-PARAFAC

愛知学院大学薬学部
生体有機化学講座
教授
神野 伸一郎 博士(薬学)
医薬品は多様な構造をもった有機化合物であるため、光などの外的因子により変化が生じるものが多く、色調変化による薬効や生活の質(QOL)の低下のみならず、分解物の生成によって副作用が発現するなど、適正な薬物治療を実施する上で問題となっている。医薬品の原薬や製剤の光安定性は、日米 EU 医薬品規制調和国際会議(ICH)で合意された新原薬及び新製剤の光安定性試験ガイドラインに基づいた試験を実施することで評価されている。その試験に要求されるデータ取得には、高速液体クロマトグラフィー(HPLC)やガスクロマトグラフィー質量分析法(GC-MS)など、多種多様な分析手法が利用され重要な役割を果たしているが、分解の経時的な変化を可視化することは難しい。
蛍光指紋は、励起蛍光マトリックス(EEM)と呼ばれ、励起波長、蛍光波長、蛍光強度の情報を三次元的にプロットした測定法で、指紋のような等高線マップは成分特有となる。また本測定法に多変量解析のParallel Factor Analysis(PARAFAC)を組み合わせたEEM-PARAFAC解析は、多成分が重なり合ったEEMを、個別の成分スペクトルに分離することができるケモメトリクス的手法である1)。農産物や食品の品質評価、水質のモニタリングへ応用が進んでいる反面2-7)、医薬品の安定性評価にはこれまでほとんど活用されてこなかった8)。本稿では、医薬品の光分解過程の可視化を目的とし、EEM-PARAFAC解析による光安定性評価法の開発に取り組んだ9)。
EEM-PARAFAC解析の適用に向けて、光安定性が低いことが知られているフェノチアジン系抗精神病薬を研究対象として用いた。まずメタノール中におけるchlorpromazine hydrochloride(1)の濃度と蛍光強度の線形性を確認した結果、5~25 μMの範囲において良好な直線性を示すことがわかった。そこで 10 μM の1 メタノール溶液に対し、365 nm のLED光を照射し、酸素雰囲気下、25℃における吸収、蛍光スペクトルを経時的に測定した(図1)。1は紫外域に吸収帯が観測され、260 nm 付近の吸収帯は、フェノチアジン環のπ-π*遷移、310 nm 付近の弱い吸収帯は、硫黄原子のn-π*遷移に由来することがDFT計算よりわかった。また450 nm 付近をピークトップとする青色蛍光を示した。LED光を照射すると、吸収帯の形が変化し、長波長側にテイルが見られ、溶液は無色からオレンジ色に変化した。また1の蛍光波長は大きくブルーシフトし、極大波長は375 nm 付近を示した。これら光照射による吸収、蛍光のスペクトル変化は、溶媒間(ジクロロメタン、アセトニトリル、ジメチルホルムアミド、水)で、ほとんど差はみられなかった。
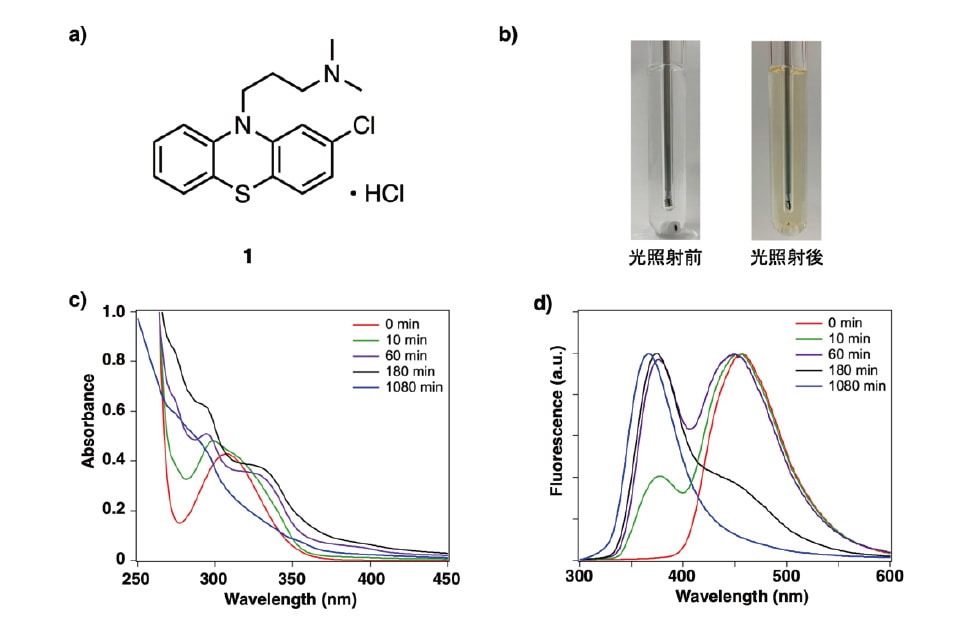
図1
a) Chlorpromazine hydrochloride(1)の構造
b) 無色透明の光照射前後の1は、光照射によりオレンジ色に呈色する。
c) 1メタノール溶液の吸収スペクトル変化。時間(min)は光照射時間を示す。
d) 1メタノール溶液の蛍光スペクトル変化。時間(min)は光照射時間を示す。
メタノール溶液における1の光分解過程をEEMで経時的にモニタリングした。光照射時間の延長に伴い、1に帰属される蛍光波長(em)450 nm / 励起波長(ex)260 nm、310 nm の等高線マップの強度が減少し、em 300-450 nmとex 200-350 nmの範囲に及ぶ新たな等高線マップが出現した。続いて、PARAFAC解析により成分スペクトルの分離を行った結果、1のem 450 nm/ex 260, 310 nm(C1)の強度が光照射30分で減弱し、em 375 nm/ex 250, 275, 335 nm(C2)とem 355 nm/ex 240, 290 nm(C3)の等高線マップが時間依存的に出現した(図2)。C3はC2より遅れて生成することがわかった。また本EEM-PARAFACモデルのCore consistency(成分数の妥当性を示す指標)は91%を示した。
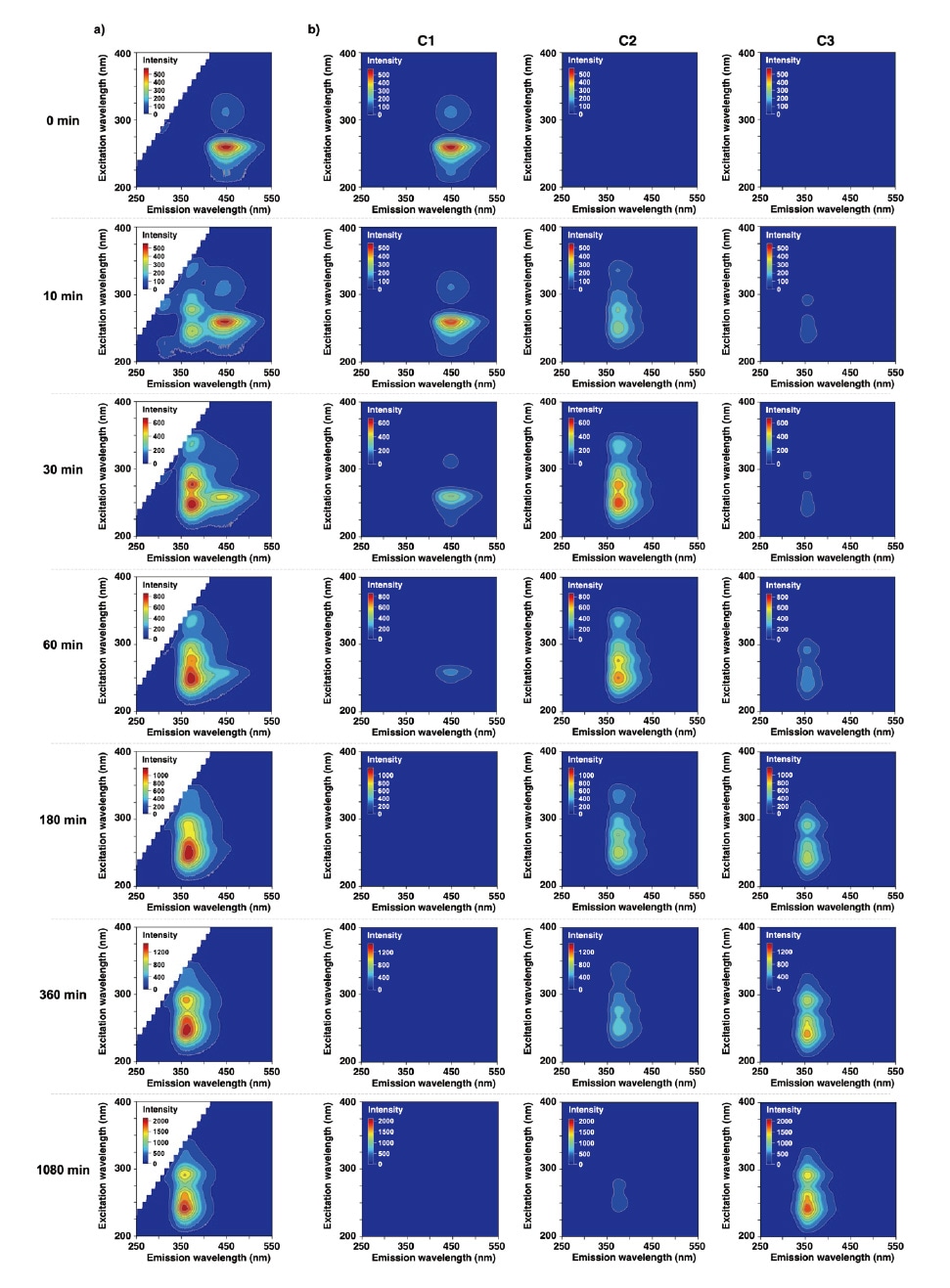
図2
a) 1メタノール溶液のEEMスペクトルの変化。時間(min)は光照射時間を示す。
b) PARAFAC解析。本モデルは3成分にスペクトル分離できた。
EEM-PARAFAC解析で分離された成分数の妥当性を更に検証するため、1の光分解反応の生成物を捕捉し、分解物の化学構造とEEMの関係を明らかにした。まず10 mM の1メタノール溶液に対して、酸素雰囲気下、365 nm のLED光を照射しながら18時間反応させ、得られた反応混合物をシリカゲルクロマトグラフィーで分離精製した。その結果、1が酸化されたphenothiazine hydrochloride sulfoxide(2)が主生成物として得られ、単結晶X線構造解析により、2の結晶構造を同定することに成功した。副生成物の2-chloro-N、N-dimethylcarbazole(3)は、NMRを用いて構造決定した。更にC17H19ClN2SOとC17H19ClN2SO3の分子式に相当する微量の酸化物がそれぞれ生成することがわかった。
続いて、単離された光分解物2と3をメタノールに溶解させEEMを測定し、PARAFACより成分分離されたC2とC3の等高線マップの帰属を行った。その結果、C2の等高線マップは、2のem 375/ex 275, 335 nmと一致し、C3の等高線マップは、3のem 355/ex 240, 265 nm, 290 nm のEEMとそれぞれ一致した(図3)。上記の結果を踏まえて、本EEMPARAFAC解析は、3成分モデルでフィッティングできることが明らかとなった。
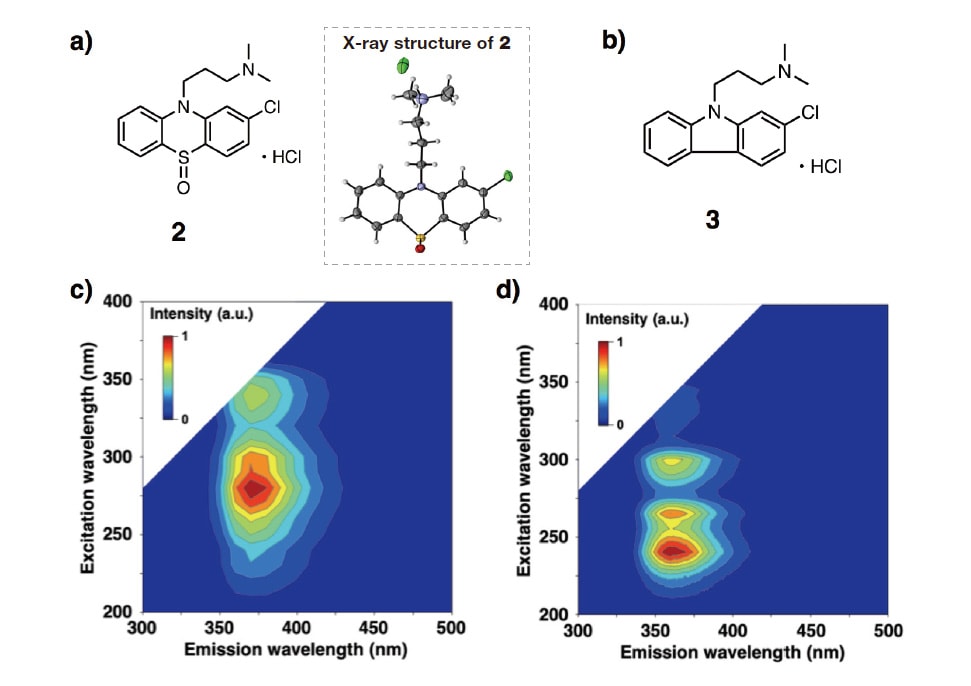
図3
a) phenothiazine hydrochloride sulfoxide(2)の化学構造と結晶構造
b) 2-chloro-N,N-dimethylcarbazole(3)の化学構造
c) 2メタノール溶液のEEMスペクトル
d) 3メタノール溶液のEEMスペクトル
続いて、1の光分解反応を定量的に把握するために、速度論的解析を行った。[1]0は1の初濃度、tは光照射時間(min)を示した。またem 450 nm/ex 260 nmのC1スコア値に着目し、光照射時間tのスコア値(It)とt = 0のスコア値(I0)から式1に基づいて、スコア変化率(Qem)を求めた。各光照射時間における1の残存濃度は、[1]0にQemを乗ずることで算出した。
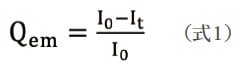
図4は、1の時間−濃度変化曲線を示す。このプロファイルから、1は一次反応に従って分解することがわかった。続いて、式2の速度式を入力したカーブフィッティングプログラムをMatplotlibで作製し、Levenberg-Marquardt法を用いて非線形フィッティングを行った結果、反応速度定数(k1)は、8.7×10-3 min-1を示し、光分解反応の半減期(t1/2)は80分となった。
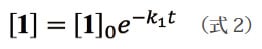
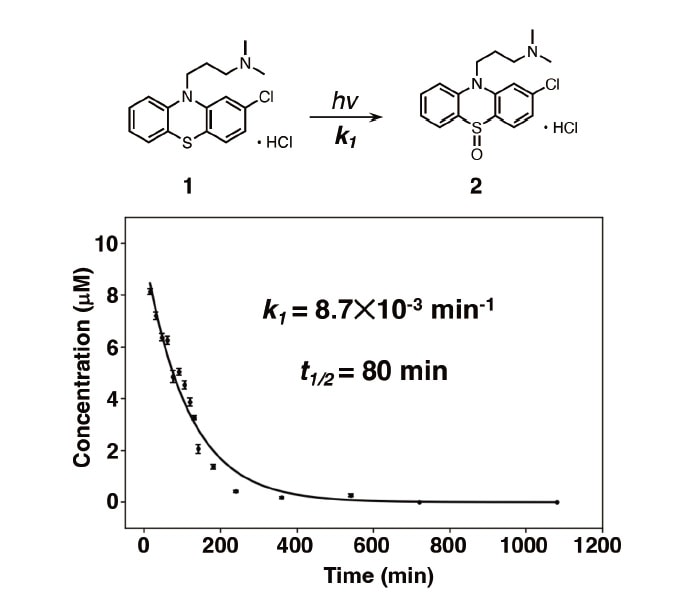
図4 光分解反応の速度論的解析
最後に、本EEM-PARAFAC解析を、側鎖構造が異なるフェノチアジン系抗精神病薬のlevomepromazine maleate(4)とprochlorperazine Maleate(5)の光安定性評価に適用した。化合物間で光分解の程度に大きな差は見られなかったが、いずれにおいても、光照射後速やかに原薬(C1)の等高線マップが消失し、sulfoxide体(C2)とcarbazole体(C3)に相当する等高線マップが現れ、光分解の経時的変化を可視化することに成功した。続いて、3成分の相対濃度を求め、濃度分布の時間的変化を調べた結果、10分間の光照射で50%以上の原薬が分解した。またcarbazole体は、sulfoxide体より遅れて生成し、光照射180分後には、55%程度の濃度分布を示すことがわかった(図5)。
以上より、EEM-PARAFAC解析によるフェノチアジン系抗精神病薬の光安定性評価法を構築した。本法は、原薬の光分解過程を等高線マップで可視化でき、HPLCやGC-MSと比較して、カラムクロマトグラフィーによる成分分離を行うことなく、原薬の光分解過程に関する定量的な情報を得ることができた。また原薬サンプルや溶媒等の使用量も大幅に低減できた。
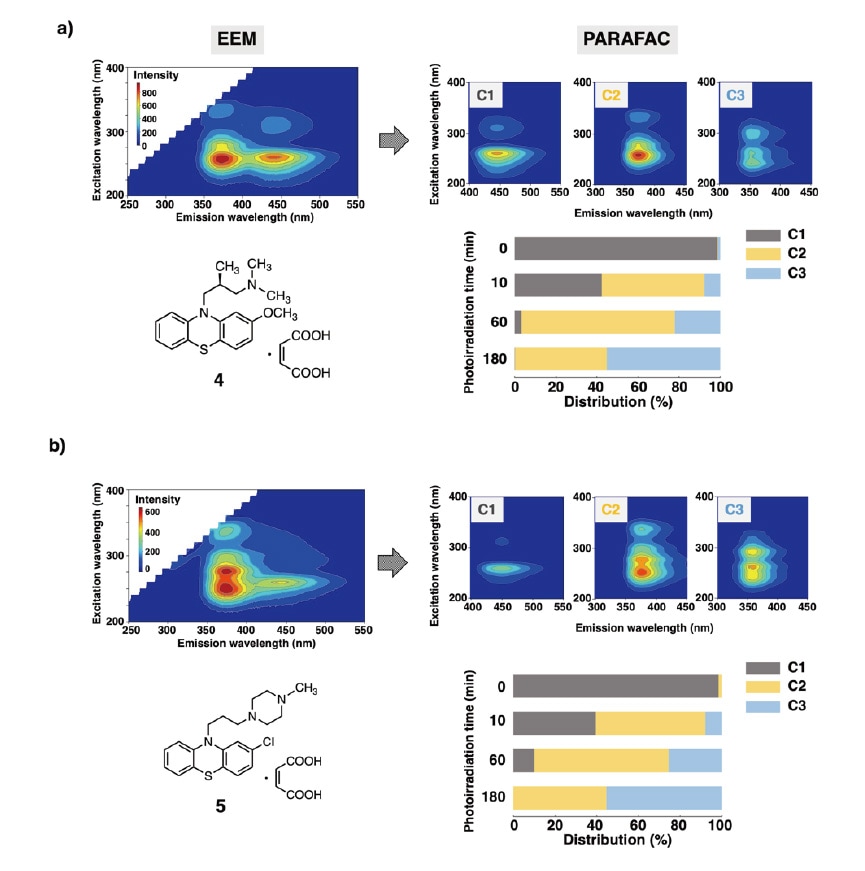
図5
a) Levomepromazine maleate(4)の光安定性
b) Prochlorperazine Maleate(5)の光安定性
医薬品の原薬や製剤の光安定性の評価には、多種多様な分析手法が利用され重要な役割を果たしているが、いずれの手法も分解の経時的な変化を可視化することは難しい。本稿では我々が開発したEEM-PARAFAC解析による医薬品の光安定性評価法について紹介した。本手法は、原薬の光分解の時間的変化をマッピングで可視化でき、光分解反応の速度論的解析やスコア値から個別の成分の相対濃度を算出することで、分解過程に関する定量的な情報を得ることができた。
薬剤師をはじめとした医療従事者は、光に不安定な医薬品を取り扱う際、原薬の光感受性に関する情報を事前に把握し、医薬品の保管、製剤の調製から治療提供に至るまで、品質を維持することが求められている。例えば、研究対象としたフェノチアジン系抗精神病薬の医薬品インタビューフォーム内には、「光によって分解変色するため、開封後は遮光して保存すること。着色の認められるものは使用しないこと」と記載され、取り扱いに関する注意が情報提供されている。一方、EEMPARAFAC解析により、本医薬品の光分解における主生成物は、無色透明な外観をもつ酸化体であることを見いだした。医薬品の安定性を確認する際、色などの外観や性状は着目しやすいため目安となるが、適正な薬物治療を実施する上で、分解物や分解経路を正しく同定することは必須である。EEM-PARAFAC解析は、それらを迅速かつ簡便に把握、理解できる有用な手法となるであろう。また医薬品等の品質管理分野におけるレギュラトリーサイエンスの実践にも貢献できることが期待される。
参考文献