Development of a new type of cryo-electron microscope for simultaneous STEM, SEM imaging and its application to biological samples
臼倉治郎*1、成田哲博*1、松本友治*1、臼倉英治*1、砂押毅志*2、丹波裕介*2、長久保康平*2、
東淳三*2、水尾考志*2、二村和孝*2、大隅正子*3、多持隆一郎*2、小瀬洋一*2
クライオ電子顕微鏡(クライオ電顕)の必要性はここ数年で急速に高まっている。その主な用途は精製タンパク質、ウイルス及び微小オルガネラの構造解析(単粒子解析)である。従来の負染色によるタンパク質分子の観察では、内部の構造解析が困難である。負染色はいわば空気乾燥であり、たとえ瞬時に染色剤が分子周囲を囲んでも構造変化を完全に防ぐことは難しい。また、染色剤の浸透具合により像も変化する。クライオ電顕では染色のような前処理をせず、精製タンパク質分子であればそのまま急速凍結して観察することになる。このため、生物試料であっても、電子顕微鏡(電顕)の分解能で観察することができる。この点は重要で、従来の超薄切片法やレプリカ法では前処理の段階で試料分解能が低下している。とはいえ生のタンパク質は極めて電子線に弱く、液体窒素温度での観察では照射電子数が約20個/Å2で試料を失うことになってしまう。このため、常時1~3個/Å2で観察しなくてはならない。最近の電子直接検出(direct detection)の高感度カメラ(DDカメラ)の発展はこれを可能にしている。また、単粒子解析は結晶化を必要とせず、分散系での構造解析が出来る。最近のチャンピオンデーターによれば分解能も3Åに達しており、結晶のX線回折による構造解析に近づいている(Meyerson et al, 2016)。しかも、このような解析が生に近い凍結状態で得られることは特筆に値する。
一方で、クライオ電顕は単粒子解析だけではなく、従来通り構造観察にも極めて有用で、凍結切片のクライオ電顕観察により細胞間接着装置であるデスモゾームや遺伝子情報に沿ってタンパク質を合成するリボゾームなどの分子構造が明らかになっている(Al-Amoudi et.al, 2004)。今後は細胞内の病態解析などにも必要な装置となるであろう。実際、インフルエンザウイルスの細胞内への取り込み過程の構造解析に利用されている(Fontana & Steven, 2015)。一般的に生命現象を理解するためには、細胞内で機能状態のタンパク質分子やその複合体の構造、それとともにそれらが集合した空間構造(いかなる構造でどのような細胞内環境に位置するかという情報)を知る必要がある。これらを新鮮状態で観察するにはクライオ電顕が必須である。しかし、日本におけるクライオ電顕の普及は欧米に比べ十分とは言えない。新鮮な組織細胞をクライオ電顕で観察するためには急速凍結装置やクライオミクロトームなどの前処理装置が不可欠である。従って、クライオ電顕で細胞を観察するには、かなりの予算(全体で約7億円程度)を必要とする。これが普及を妨げている一番の原因であろう。しかし、医学生物学の今後の発展に必須であれば設備せざるを得なく、欧米の主要大学では設置が急速に進んでいる。前処理装置を含めクライオシステムの開発が全てEUを中心に進められ、日本の貢献が少ないことも残念である。後発ではあるが、我々は市場に出回っていない、多様性に富むクライオ電顕の開発をおこなっているので紹介する。
医学生物学の全領域において、誰もが様々な場面で容易に使用できる低加速電圧クライオSTEMの開発を目指した。特にSTEM機能を持つSEMを開発ベース機とすることで、STEM像とSEM像の同時計測ができる次世代型走査透過クライオ電顕を開発した。一方、電顕開発はその応用法と一体で考える必要がある。如何に高性能な観察機器を開発しても、試料を最適な形で持ち込まない限り、性能は発揮されないし、観察結果の信頼性も薄れる。したがって、機器開発と標本作製技術開発はいわば車の両輪である。今回、我々は膜細胞骨格を観察するための前処理装置である細胞膜剥離装置の開発もおこなった。
国費を調達した研究開発としては、世界一のクライオ透過型電顕(クライオTEM)を目指すべきところであるが、すでにユーザーフレンドリーな300 kVクライオTEMが存在し、チャンピオンデーターを出している現実がある。大変高価という欠点はあるが、これを凌ぐ機器の開発には多くの要素技術開発が必要であり、多額の費用がかかる。我々が現在受けている日本医療研究開発機構(AMED)からの支援だけでは難しい。これが原子分解能を目指さない主な理由であるが、本研究課題であるSTEM、SEM同時計測の低加速電圧クライオ電顕開発も優れた点が多々あり、今後の開発研究次第ではダークホースとなりえる。例えば、一般にクライオTEMで生物の凍結試料を観察すると正焦点ではコントラストが極めて低いため、under側へピントをずらし位相コントラスト(フレネルコントラスト)を生じさせ観察する。これは電顕本来の分解能を低下させることになる。このような画像データーをもとに単粒子解析を行うには、コントラスト伝達関数(CTF)の補正とともに多くの画像データーが必要となる。我々の開発機では走査電子顕微鏡(日立ハイテク製SU9000)のSTEM光学系をそのまま使用して透過像を得ている。STEMでは極めて細いビームで走査し、試料を透過した電子の密度分布が画像となる。要するにレンズによる結像ではなく、電子密度のビットマップが画像となるので、CTFの影響を最小限に抑えることが出来る。当然のことながら正焦点での像観察も可能であり、分解能の低下も抑えられる。したがって、単粒子解析には有利で、TEMに比べ、比較的少数の画像データーですむ。もう一つ大きな違いは画像の記録法にある。TEMでは画像を記録するためにカメラが必要であるが、STEMでは電子を捕捉するためのシンチレータがあれば良い。今後の研究開発次第ではこの差は重要な意味を持ってくるかもしれない。現状では、クライオTEMに取り付けて使用するCMOSからなるDDカメラが圧倒的に優れている。しかし、カメラ単体で1億円近くする高価なものである。一方、STEM用のシンチレータは電子を捕捉するだけであるから、フォトンカウントできるほどの高感度化であれば良い。例えば、蛍光物質を厚く塗るなどして、もし1電子を捕捉できるほどの高感度化が実現できれば、DDカメラよりも遙かに安く、同等の像が得られることになる。今後の研究開発の結果に依存している。特別な電顕室を作る必要がなく、研究室の片隅に設置しただけで、1 nm程度の分解能で単粒子解析が容易にでき、また、生きている状態に近い細胞内微細構造も観察できるとなれば、大多数の医学生物学の研究者は満足するはずである。このような特長のクライオ電顕の開発を目指した。
クライオトランスファーホルダーの開発は開発計画の中で最も重要な要素技術である。ホルダーアームの2/3ほどを真空二重パイプ化し、液体窒素を先端近くまで満たすことにより、冷却速度を上げることができた。さらに、充填した液体窒素から脱気するための真空システムを追加し、液体窒素をスラッシュ化することを試みた。これにより、最終的に-190℃の低温を達成した。クライオトランスファーホルダーでスラッシュ窒素を利用するのは世界で初めての試みであった。さらに、液体窒素のIN/OUTの経路を最適化したことにより、冷却速度の向上および冷却効率の向上をはかった。本ホルダーを-180℃に温度制御することで実試料測定が可能となった。しかし、-185℃近辺ではクライオトランスファーホルダーの温度変動による画像ドリフトが激しく、長時間の観察が困難であった。これは、クライオトランスファーホルダー先端に配置されたステージとの接触部からの熱浸入によるものである。したがって、非接触タイプのステージの開発をすることで画像ドリフトが低減し長時間の観察を行なうことが可能であると判断する。
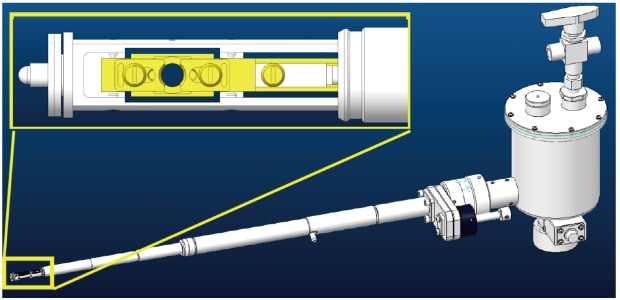
図1 試作クライオトランスファーホルダーのCAD図 左上は先端の試料ホルダー部の拡大
クライオ電顕では試料が極低温下にあるため、試料へのコンタミネーションを防ぐために試料温度以下に冷却されたコンタミネーショントラップが必須である。トラップのアーム部分もパイプ化を施し、先端近くまで液体窒素が流入できるようにした。さらに、排気システムを追加し、窒素をスラッシュ化することにより-200℃まで冷却することに成功した。トラップ先端はクライオトランスファーホルダー先端の試料部分を包み込むような形状に設計した。また、これに付随し、顕微鏡本体(SU9000)のバッファタンクを冷却することで、試料室の真空度2×10-6 Pa(従来:7×10-6 Pa)を達成した。これらの改良により、試料上への再氷結をほぼ完全に防ぐことができた。
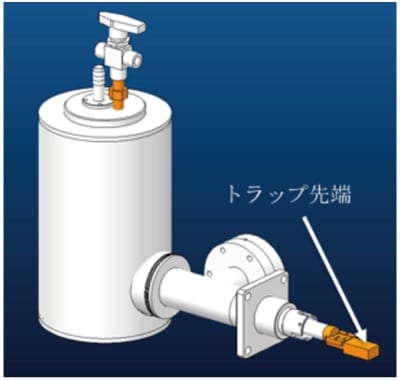
図2 アンチコンタミネーショントラップのCAD図
スラシュ化窒素を用いることにより-200℃まで冷却することに成功した。トラップ先端部は試料ホルダーの先端部(試料部分)を包み込むように設計されている。
前述のように高性能な観察機器でも、試料処理を誤れば、機器の性能も引き出せないし、信頼性のある観察結果も期待できない。機器開発と標本作製技術開発は表裏一体である。クライオ電顕観察の前処理技術も残念ながら欧米に後れをとっている。試料を急速凍結し、クライオ切片を作り観察するというオーソドックスな方法は全て欧米で開発された。全部揃えると1億円近くする前処理装置群が存在する。我々はあえてオーソドックスな凍結切片法をとらずに、背側の細胞膜を剥ぎ、腹側の細胞膜に付着する膜細胞骨格をクライオ電顕で観察することを考えた。そこで、freeze-etching法の前処理としてすでに使用されていた超音波によるunroofing(細胞膜剥離)法の改良、再開発をおこなった。この方法では、細胞内の可溶性成分が流出するが、それにより細胞骨格などの構造体は相対的にコントラストが増加するはずである。実際、膜細胞骨格やオルガネラを高コントラストで観察できた。この方法により処理された試料は膜の細胞質側表面を俯瞰できるなど予想以上の成果があった。しかし、市販のプローブ型超音波発生装置をそのまま使用したのでは出力が強すぎ、電顕用のメッシュに張られたカーボン支持膜上で培養した細胞に適用すると、支持膜ごと細胞が破壊されてしまうなど、再現性に問題があった。そこで、どの程度の出力が適当であるのかを調べた結果1 W以下でなければならないことがわかった。一般に市販されているプローブ型の超音波発生器は50 W以上で、5 W以下の出力制御は困難である。そのため、出力が5 W以下で0~1 Wでも制御出来る装置をメーカーに特注した。細胞膜剥離装置はこの特注の低出力超音波発生制御装置のほか超音波発生プローブを試料に正確に近づけるためのポジションコントローラー及び細胞膜剥離過程を観察するための実体顕微鏡から構成されている(図3)。これにより、細胞膜剥離が極めて容易になった。また、クライオ電顕だけでなく、その他の観察機器の標本作製法としても有用であることが分かった。特に原子間力顕微鏡(AFM)では細胞内の構造観察は難しいと考えられていたが、細胞膜剥離標本を用いることで細胞内の構造を水中で初めて観察することに成功した(Usukura et al. 2016)。図4は本開発機を用いて、標本をつくり、AFMで観察した像である。細胞内(in situ)でアクチン1本1本の分子構造解析も可能である。

図3 試作した細胞膜剥離装置の正面写真(左)と斜めからの近景写真(右):低出力プローブ型超音波発生装置、プローブのポジションコントローラー、実体顕微鏡、水平照明装置から構成されている。矢印は超音波発生用プローブ、アステリスク(※印)は水平照明装置
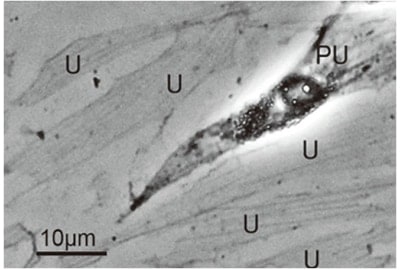
図4 細胞膜剥離後の細胞の位相差光学顕微鏡像
腹側の細胞膜上に細胞骨格(ストレス線維)が載っているのが観察される(U)。PUは部分的に細胞膜が剥離された細胞を示す。

図5 NRK培養細胞の細胞膜の裏打ち構造。BはAの四角に囲んだ部分の拡大図。アクチン線維の短周期構造が容易にわかる。CL:クラスリンコート、CV:カベオラ、アステリスク:細胞膜に密着する滑面小胞体
開発当初の目的であった無固定新鮮状態の膜細胞骨格のクライオSTEM、クライオSEMの同時計測については、現在ではほぼルーチンに観察できるようになった(図6)。細胞膜剥離により可溶性タンパク質を流出させているため、十分なコントラストが得られるので、不足焦点ではなく正焦点での観察が可能であった。また、細胞膜剥離後も予想以上にリボソームや小胞体も残っており、膜細胞骨格のみならず、様々な構造が観察された(図7)。中には細胞膜のほんの一部だけが破損していると思われる細胞では、まだ可溶性成分がかなり残っているにもかかわらず、十分なコントラストで観察できた。30 kVの低加速電圧にもかかわらず、厚さが200 nm以上と推定される部分でも、支障なく観察できたのはうれしい想定外であった。これがSTEM光学系の特徴なのか否かは分からないが、生物試料では30 kV加速電圧でもSTEMで細胞内構造を支障なく観察、計測できることが分かった。これは今後新しいタイプの電顕を開発する上で、重要な一歩である。
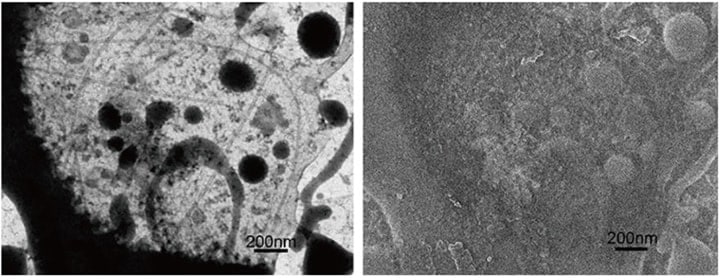
図6 クライオSTEM(左)とクライオSEM(右)の同時記録(無固定)
完全に氷包埋されている時(最初)、SEM像は氷で覆われているので平坦であるが、電子線照射によるダメージや温度を上昇させ、氷の一部を昇華させると右図のように構造が現れる。
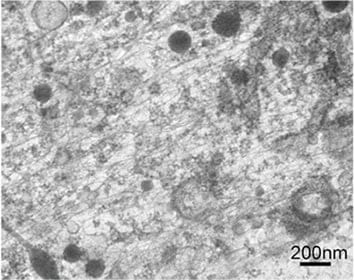
図7 膜剥離標本のクライオ電顕像(無固定)アクチン線維や微小管からなる細胞骨格に加え、粗面小胞体、滑面小胞体、リボゾームなどが観察される。
もうひとつ本開発プロジェクトの応用研究で明らかになったことがある。それは最初に述べたとおり、STEMでは対物レンズが直接結像に関与しないため、単粒子解析には最適であることが判明した。特に本開発機はcold FE電子銃を装備しているため、ビーム径が細く、この傾向がさらに強い。実際、アクチンフィラメントの分子構造解析において、通常の100 kV透過型電子顕微鏡写真から求められた分子構造より、さらに高分解能の分子構造をわずか20枚程度の画像から導き出すことが出来た(図8参照)。少数で分子構造解析できると言うことは分離精製タンパク質ではなく、細胞内に散在する少数の標的分子の構造解析ができることを意味しており、本機器開発の方向性が正しかったと考えられる。アデノウイルスの負染色像の解析に用いた場合も同様で、少量で十分な解析結果が得られた(図9)。
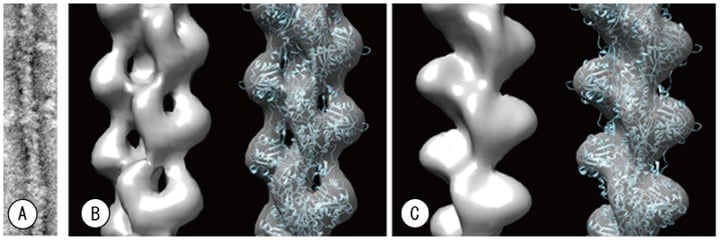
図8 開発機と通常のTEMとの比較。負染色像(A)から、ラセン対称性を考慮した単粒子解析により三次元再構成を行った。(B)開発機30 kV STEM。(C)通常の100 kV TEM。
原子座標モデル(Oda et al. 2009)とのフィッティングを行った結果、通常の100 kV TEM像から三次元再構成した像(C)では合致しない部分が存在するが、開発機STEM像から三次元再構成した像(B)では大変良く一致していることが分かる。
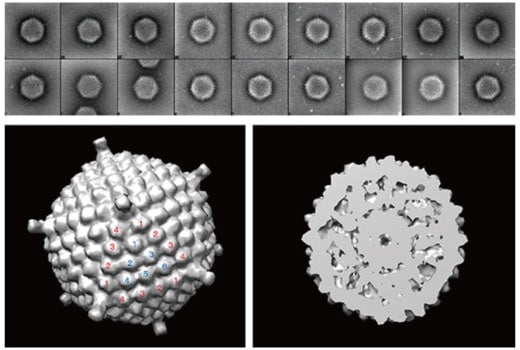
図9 開発機を用いて撮影したアデノウイルス粒子像18個(上部)からの再構成
クライオトランスファーホルダーを用いたクライオ電顕は主として生物の凍結試料を観察するために開発されたが、照射ダメージを軽減する効果もあるので材料系でも今後は使用されるだろう。少しややこしいがクライオホルダーを用いたクライオ観察は材料系でも以前から行われていた。トランスファーという用語が使われていないのは電顕に挿入してから、冷却を始めるからである。金属などでは問題にならないが、水を含むものでは結晶状の氷が出来てしまい使い物にならない。そのため、生物材料では急速凍結によりアモルファス氷(非晶質)としてから、凍ったまま電顕に持ち込むのでトランスファーの一語が追加されている。氷(結晶)は液状の物質では重要な問題である。最近、我々は水の中に形成されるナノバブル(100 nm前後の気泡)の観察に成功した(図9)。これは従来のクライオTEMでも観察できると思うが、我々の開発機ではSTEM、SEM同時観察が可能であることから、実際にバブルが水の中に存在することを証明できる。これは新たな利用法であり、今後、化粧品、医薬品、食品、ソフトマテリアル部門の研究所等での本開発機の需要が見込まれる。
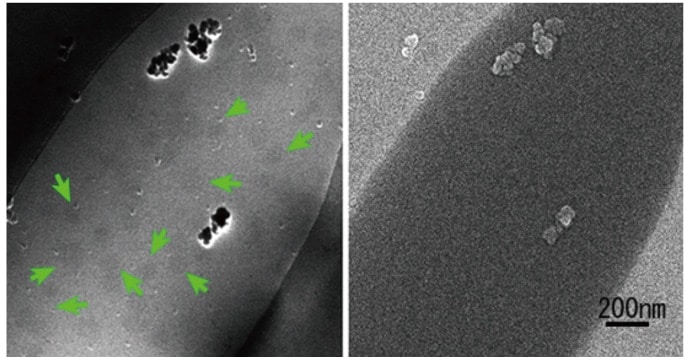
図10 開発機で捉えた水中に生じたナノバブル。QUANTIFOILの膜穴に水を張って急速凍結し観察した。左がクライオSTEM像。右が同時に撮影したSEM像。矢印はバブルを示す。透過像ではバブルは黒く見えることが多いが、相対的なもので、白っぽく見える時もある。
SEMを開発ベース機とした関係で、現時点ではSEMに付随しているSTEM機能を用いているが、将来的にはSTEMを中心に設計し、それに高機能SEMを付帯させるのが望ましい。クライオ電顕で通常の電顕の画質を維持するには、冷却に伴うドリフトが顕在化しないよう走査速度を上げたい。AFMでは10年前には高分解能記録だと1フレームに20分もかかっていたが、今では10秒/フレームが標準になりつつある。一方、SEMの記録時の走査速度は30年間変わっていないのが実情である。電顕で走査速度を上げるにはプローブ電流を増やすのが正攻法であるが、試料ダメージが懸念される。検出系の高感度化と最新のドリフト補正技術を組み合わせることで、高倍率で高画質なクライオ電顕像の形成を目指す。
謝辞
本研究は国立研究開発法人日本医療研究開発機構(AMED)の医療分野研究成果展開事業(先端計測分析技術・機器開発プログラム)の支援によって行われた。
参考文献
さらに表示