Observation of Solution Samples by Transmission Electron Microscope

北海道大学 低温科学研究所
准教授
木村 勇気 博士(理学)
1931年にベルリン工科大学のルスカ等を中心として開発された透過型電子顕微鏡(TEM)は、「より小さな物体を観察したい」、「より細かい情報を得たい」という我々の欲求を満たしてくれた。その後、当然のように「動的なプロセスを時間を追って直接観察したい」、「より現実に近い環境で観察したい」という次の欲求が生まれた。前者は、加熱ホルダーや冷却ホルダーなどの登場によって実現され、近年のカメラの発展により、分解能を保ったまま高速で現象を捉えられるようになってきた。後者に対しては、
その後、溶液ホルダーが米国のProtochips社やHummingbird Scientific社から市販されると、例えば我々の分野では“微結晶が方位をそろえて接合する成長過程”2)や“炭酸カルシウムの結晶化前の非晶質粒子の出現”3)が示されるなど、溶液中での結晶化過程をTEM観察する研究が世界的に盛んに行われるようになった。また、リボソームやロタウイルスなどの生物試料の観察報告も増えており4)、研究分野を広げている。特に、これまでTEM観察には凍結や染色が必須であった生体試料においては、溶液TEMは実環境下でのサイズや形を評価できる強力な手法であるといえる。溶液サンプルに対してTEMの強力な機能を適用できるようになり、材料科学、自己組織化、電気化学や触媒作用、ナノ粒子の成長、流体物理学、放射線物理学、粘土やエアロゾルを含む地質学および環境学、複雑な生体材料やポリマー、生物学、創薬、食品、塗料や化粧品などの非常に多くの分野でブレークスルーが起こる可能性を秘めていると考えている。我々のグループでも、金属ナノ粒子、光触媒粒子、コロイド粒子、塩、タンパク質、粘土鉱物、セメント、リボソーム、大腸菌など様々な試料の観察をしてきており、その大きな可能性を実感している5-8)。
現在は、DENS solutions社からも溶液ホルダーが販売されており、また、既存のホルダーを利用できるK-kit(Materials
Analysis Technology Inc.)と呼ばれる溶液セルも登場し、利用しやすくなってきた。我々は、2012年にProtochips社の溶液ホルダーを日立の加速電圧200 keV、LB6フィラメントのH-8100に導入し、試行錯誤しながら手法を確立しつつ(身内ではフルイド反応TEMと呼んでいる)、Protochips社と意見交換を続けてきた。そのため、ここではProtochips社のPoseidonと名付けられている溶液ホルダーに関して述べる。特に、溶液ホルダーの導入を検討する際に知りたいと思われる情報をできるだけ盛り込むよう努めた。
溶液は、シリコン製の窓付き板2枚(製品名:E-chips)の間に封入することで、TEMの真空環境に導入できる(図1)。窓付き板の中央には切欠きがあり、30-50 nm厚の非晶質窒化シリコン膜が窓として用意されている。静止(Static)や混合(Flow)と名付けられた小さな窓付き板(2.0×2.0×0.3 mm)には、図1Bに金色で見られるようなスペーサーが用意されており、この厚みを選ぶことで、異なる溶液厚さ(50 nm-5 µm)を準備できる。我々は普段、試料の数密度とコントラストの関係から、150 nm、または500 nmのスペーサーを用いている。電子線はこの窓を透過することで溶液を観察できる。また、スペーサーが四隅に柱のように用意されているFlow E-chipsを用いれば、TEM観察下で二種類の溶液を混合したり、異なる溶液を流して反応条件を変化させたりできる。マイクロウェルと呼ばれるE-chipsは、窓の中央に井戸がいくつも掘られたような構造をしている。スペーサーはなく、この井戸の中に溶液を封入して観察することになる。井戸の底だけが薄い非晶質窒化シリコンであるために、TEMの真空による溶液層の膨らみを低減でき、よりクリアな像を得ることができる。また、加熱用の窓付き板(大)(6.0×4.5×0.3 mm)を用いることで、室温から100℃まで温度制御も可能である。溶液は、特殊な形状をしたガスケットによりTEMの真空から隔離される。ガスケットは、耐薬品性を考慮して、バイトン、EPDM、パーフロから、試料に応じて選択できる。現在のPoseidonホルダーは、TEMの傾斜機能を用いることで、エネルギー分散型X線分析(EDS)にも対応している。
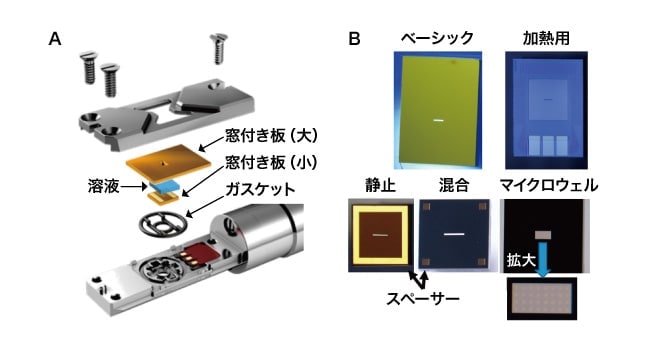
図1 Protochips社(米国)の加熱機構付き溶液ホルダー(製品名:Poseidon)先端の模式図(A)と、非晶質窒化シリコンの薄膜を窓に持つシリコン製の板(E-chips)の光学顕微鏡写真(B)
大小の窓付き板にはいくつかの種類があり、用途に応じて使い分けることができる。現在、400を超える組み合わせが可能である。溶液内部は、電子線がこの窓を透過することで観察できる。
購入時のE-chipsには、非晶質窒化シリコンの膜上に保護膜が貼ってあるので、アセトンとメタノールを用いて洗浄した後にエアダスターで乾燥させる。その後、溶液を均質にE-chips上に載せたり、スムースに流したりできるようにE-chipsの親水化処理を行う(図2)。すると、水溶液の場合、図2Cに示すように、非常に濡れが良くなる。非極性溶媒を使うときなど、窓付き板を150℃で1.5時間加熱することで疎水処理もできる。

図2 溶液セルを組み立てる前に行う親水化処理の様子(A)、および30秒間親水化処理する前(B)と後(C)で同量の水を滴下した様子
親水化後には、窓付き板が一様に濡れていることが分かる。
図3に溶液セルを組み立てる様子を実体顕微鏡写真で示す。Aに見られる特殊な形状のガスケット上に窓付き板(小)を載せ(図3B)、溶液を0.5 - 1 µL程度滴下する(図3C)。上から窓付き板(大)をかぶせて(図3D)、チタン製の蓋で覆い、トルク管理をしながらネジ止めする(図3E)。窓の長手方向を90°異なる向きで設置すると、図3Fの中央に明るく見られるように、50×50 µmの観察領域が準備できる。窓が割れていたり、異物が挟まっていたりすると、実体顕微鏡で拡大して観察した際に、窓が不均一な干渉縞を示すために、直ちに分かる。最終的な溶液量は、500 nmのスペーサーの場合2 nL程度である。

図3 Poseidon用の溶液セルの組み立て手順
TEMの鏡筒内に溶液をまき散らさないために、観察前に必ずリークチェックを行う(図4A)。但し、TEM内で溶液がセルからリークしても、真空計の針はほとんど振れず、混合セルを用いて溶液を流し続けていなければ、TEM本体に与える影響も限定的であると感じている。溶液を流す場合には、内径100 µmのPEEKチューブでシリンジポンプとつなぐ。廃液は内径150 µmのPEEKチューブを通してビーカーなどに排出する。図5に溶液セルの観察窓領域のTEM低倍率像を示す。四隅が明るいことが分かる。これは、TEMの真空により非晶質窒化シリコン膜が引っ張られているためで、中央ほどその影響が大きい。そのため、通常の観察は四隅を中心に行うことになる。

図4 観察前に行うリーク(水漏れ)チェックの様子(A)とTEMに導入した様子(B)
溶液を流す場合にはPEEKチューブでシリンジポンプとつなぐ。

図5 溶液セルの観察窓領域のTEM低倍率像
図6に水を金のコロイド溶液で置き換える様子を示す。スペーサー150 nmのFlow E-chipsを用いて、金コロイド溶液を2 µL min-1で流すと、水が徐々に金コロイド溶液に置き換わる様子が見られた。その際、図6のBやCに顕著に見られるように3つの異なるコントラストを持って、それぞれが同じ速度(~40 nm s-1)で右上から左下に移動した。この3つのコントラストの違いは、メニスカスが原因であると考えている(図6D)。金コロイド溶液を拡大すると、金ナノ粒子を観察することができる。これは、当たり前のように聞こえるが、実は水中の金ナノ粒子のブラウン運動による移動速度を見積もると、カメラの露光時間内に視野の端から端まで容易に動けるほどである。それにもかかわらず観察が可能であるということは、薄い水の層に存在するナノ粒子の拡散速度(移動速度)は、バルク液体から予想されるよりもはるかに小さいことを示している。その不一致は、7 - 9桁にものぼる。これは、細孔内の水中のナノ粒子の拡散を予想する計算でも説明できない。しかし、このような非常に大きく減衰された拡散運動のために、我々はナノ粒子の液中“その場”観察が可能なのである。

図6 Aの左下半分ほどのコントラストの弱い領域に存在する水が、徐々に右上から流れてくる金コロイド溶液に置き換わる様子
Bに示すような4段階のコントラストの違いは、Dに示すように金コロイド溶液と水との界面に作られたメニスカスが原因と考えられる。窓付き板(小)は、150 nmのスペースを持つ混合(Flow)を用い、流速2 µL min-1で金コロイド溶液を流した。
我々の研究の一例として、コンクリートの劣化を防ぐために使われるシリカ粒子とCa(OH)2溶液を用いて単純化したコンクリート化の初期過程の様子を図7に示す5)。Ca(OH)2溶液を流速1 µL min-1で流しながらシリカ粒子を観察すると、シリカ粒子が水和によって大きく膨らんでいく様子が見られた。個々のシリカ粒子のコントラストの積分値から、シリカ粒子は膨潤しながら僅かに溶けていることも分かった。その後、C–S–Hと呼ばれるカルシウムケイ酸塩水和物(CaO·2SiO2·4H2O)が生成した(図7D)。この観察で、C–S–Hが形成するよりも前に、シリカ粒子の膨潤によってコンクリート内の細孔が埋められていき、その後、C–S–Hが形成して粒子同士をつないでいくことで固化が進むプロセスを捉えた。シリカ粒子が膨潤する典型的な速度は~3×10–2 nm s–1であった。溶液セルを用いた実験により、他の手法ではほとんど不可能である個々のナノ粒子の水和による膨潤や溶解、成長の微小な速度を求めることが可能になった。
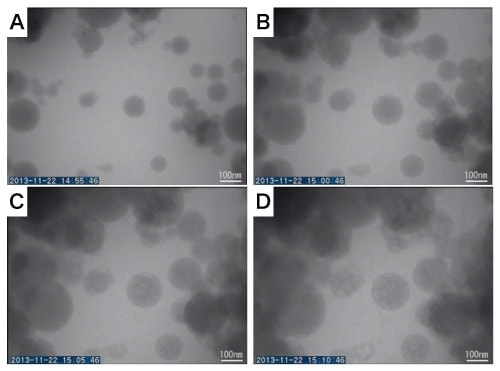
図7 非晶質シリカ粒子を溶液セル内に封じ込め、Ca(OH)2溶液を流すことで実施した、水和の様子とセメント反応の模擬実験のTEM中その場観察結果
窓付き板(小)は、500 nmのスペースを持つ混合(Flow)を用い、Ca(OH)2溶液は流速1 µL min-1で流した。
通常の観察を行った後には、膜が正常な状態であったかを、実体顕微鏡で確認している。その後、図3の組み立て手順とは逆の手順でセルを解体する。溶液を流して物質の形成過程を観察するような実験を行った際には、析出物がPEEKチューブ内で生成して、詰まりが生じるのを防ぐ必要がある。一度析出物が生成すると、難溶性の物質でなくても溶かすのは容易ではない。溶液を流す実験を行った後には、超純水を長時間流し続けることで、乾燥による固体物質の析出を抑えることが重要である。ただし、最新のPoseidonホルダーでは、ホルダー内部のPEEKチューブを自分で交換できるようになったため、以前ほど気を遣う必要はなくなり、よりチャレンジングな実験が可能になった。
Poseidonを使い始めた当初は、様々な方法で使用後のE-chipsの洗浄を試みたが、例えば超音波洗浄を行うと、観察窓は非常に薄いために直ちに破れてしまうなど、再利用するのは難しいという結論に至り、現在はすべて使い捨てにしている。MEMS技術の進歩により、様々な溶液セルが可能になってきており、価格も下がってきているため、我慢できるようになってきた。
溶液セルが登場して間もなく15年である。日本の顕微鏡学会での液中発表に関する発表はまだ限られているが、海外の顕微鏡学会では、液中観察のセッションも用意されるなど、ここ数年で大きな賑わいを見せている。ただし、新しいものに飛びつき、取りあえず観察してみたという発表が非常に多い。これに対し、現在最大の課題となっている、電子線損傷の問題に丹念に取り組んでいるグループもある。例えば、加速電圧300 keVのTEMを用いて半径1 µmの領域を1 nAの電子線で観察した時の単位時間当たりの吸収線量は7.5×107 Gy/s程度である9)。これは、一般的な放射線源が作り出す値よりも7桁も大きい。溶液TEMにおいては、電子線の影響を慎重に評価することが欠かせないのである。今後、電子線の影響の理解が進み、より簡便に評価できるシステムが構築されると期待している。その時、上記で示したような様々な分野におけるブレークスルーがより実現されていくであろう。
参考文献
さらに表示