New Platform for Protein-Protein Interaction-Based Affinity Reactions: Spongy Monolith Stationary Phases for Affinity Chromatography

京都大学 工学研究科
材料化学専攻
教授
大塚 浩二 工学博士
バイオ医薬品、特に抗体医薬品は、特異的な治療効果、低い副作用、体内での高い安定性などの利点を有することから、近年急速に開発が進められている。2018年ノーベル生理学・医学賞を受賞された本庶佑博士らによって開発されたニボルマブは、悪性黒色腫(非小細胞肺癌・腎細胞癌)治療に適用される抗体医薬品(商品名:オプジーボ)として脚光を浴びている。
通常細胞培養によって得られる抗体は、煩雑な前処理と複数の精製過程を経て単離されるが、抗体医薬品開発においては、年間数百kg以上のターゲット抗体が必要とされ、大量精製に対応した高速技術が求められている。また、新薬開発段階における抗体のスクリーニングでは、多検体の迅速分析が必要になる。精製、分析のいずれについても、一般にタンパク質間の特異的相互作用を利用したアフィニティークロマトグラフィーが分離手法として用いられている。架橋アガロースにprotein Aを固定化した分離剤を用いる免疫グロブリンG(IgG)の分離はその代表例であるが、現行以上の高い通水性や低コスト化を実現するのは難しい。すなわち、開発途上にある分離・精製過程の簡便化、高速化、低コスト化が、抗体医薬品の急峻な普及に対するボトルネックになっていると考えられる。
我々は、汎用の比較的安価な合成樹脂を用いて、超高通水性の多孔性樹脂であるスポンジモノリス(SPM)を利用した新規アフィニティクロマトグラフィー用カラムの開発を目指した研究を進めてきた。通常の粒状充填剤とは異なり、柔らかい素材であるSPMを用いることで操作性が格段に向上し、簡便なカラム作製が可能となる。さらに、SPMは連続する大きな貫通孔(10マイクロメートル以上)を有するため、低い負荷圧を保ったままで通常の10倍以上の通水速度が実現できる。
ここでは、タンパク質が結合可能なエポキシ基を含む新規SPMとしてエチレン-グリシジルメタクリレート共重合体(PEGM)基材のSPMを開発した。このSPMを液体クロマトグラフィー(LC)用カラムに充填した後protein Aを固定化(ProA-SPM)し、IgGの高速分離を試みた。同様に、pepsinを固定化したSPMカラム(Pep-SPM)も作製し、抗体のオンライン消化への適用を検討した。

図1 スポンジモノリスカラムの概念図 原材料・SPM外観・SPM内部・充填カラム・タンパク質相互作用イメージ
標的タンパク質であるIgGを用いてProA-SPMを評価した結果、グラジエント溶出条件において、中性から酸性に移動相を変化させることで、IgGのピークを得ることに成功した。牛血清アルブミン(BSA)を試料とした場合、BSAは溶媒ピークと同時間に溶出したことから、protein A-IgGの特異的相互作用が発現したと考えられる。作製したProA-SPMの有用性を評価するために、高流速下における評価を行ったところ、市販のLC用protein Aカラム(ProA-Column)では、流速の増加とともにフロースルーピークが出現したのに対し、ProA-SPMでは、9.0 mL/minの高流速条件下においても良好な回収率が得られた。さらに、Pep-SPMにおいては、比較的高流速条件(100 mL/h)においても、良好な抗体の消化が確認された。以上のことから、今回開発した新規スポンジ材料は、アフィニティ反応の新規プラットフォームとして有効であることが示唆された。
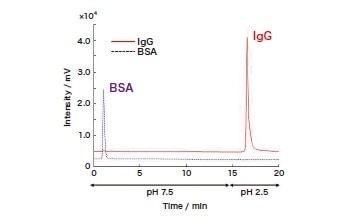
図2 ProA-SPMカラムによるIgGの特異的保持
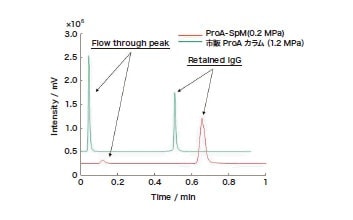
図3 ProA-SPMカラムによるIgGの高速分析(流速9.0 mL/min)
本研究の成果は、急速に開発が進む抗体医薬品の分離・精製プロセスの簡便化、高速化、低コスト化に寄与することが期待される。また、タンパク質間反応の新規プラットフォームとしての可能性も示唆されたことから、バイオ医薬品開発の迅速化や新規抗体の構造解析にも有用であると考えられる。
本研究は、筆者の研究室の久保拓也准教授を中心に展開されたものである。
参考文献
K. Kubota, T. Kubo, T. Tanigawa, T. Naito, K. Otsuka, Sci. Rep., 7, 178(2017).
さらに表示